УЛЬТРАЗВУКОВАЯ ДИАГНОСТИКА ИЗМЕНЕНИЙ МЯГКИХ ТКАНЕЙ В ОБЛАСТИ ПОСЛЕОПЕРАЦИОННОЙ РАНЫ
А.В. Гаврилин, Ю.А. Степанова, А.О. Жуков, С.В. Федотов
ГУ Институт хирургии им. А. В. Вишневского РАМН, Россия, Москва
В статье представлено динамическое УЗ — наблюдение за состоянием мягких тканей в области послеоперационной раны у 165 пациентов для определения рациональной тактики ведения пациента в послеоперационном периоде. Пациенты разделены на три группы: I — после оперативного вмешательства по поводу хирургической патологии органов брюшной полости и забрюшинного пространства; II — после грыжесечения с комбинированной пластикой сетчатым эндопротезом (Surgpro-mesh); III — после аллопротезирования аорты, магистральных артерий нижних конечностей, шеи. Всем пациентам после оперативного вмешательства проведено УЗИ мягких тканей брюшной стенки, нижних конечностей и шеи в В-режиме с целью выявления патологических изменений, с определением размеров, структуры и указанием локализации относительно поверхности кожи; в 5 наблюдениях при подозрении на наличие инфицирования процесса проводили дуплексное сканирование мягких тканей вокруг выявленного очага; при выявлении патологических изменений вокруг сосуда или протеза после протезирования магистральных сосудов выполняли дуплексное сканирование для определения гемодинамической ситуации в сосуде или протезе. Данные проведённого исследования свидетельствуют о специфике послеоперационных изменений, характерных для различных оперативных вмешательств, выявление которых даёт возможность хирургам определить тактику рационального ведения больного и уменьшить риск гнойных осложнений в области послеоперационной раны.
Введение
Заживление раны мягких тканей после оперативного вмешательства происходит естественным путем через изменения в лимфатических капиллярах с развитием отека и жидкостных скоплений большей или меньшей степени выраженности. В раннем периоде, особенно в период развития грануляционной ткани, вновь образующиеся капилляры имеют более хрупкие и проницаемые стенки, чем зрелые, легко подвергаются разрывам при незначительном натяжении ткани и даже в связи с колебательными движениями крови. В местах развивающихся микрососудов часто выявляют кровоизлияния. Самоочищение раны проходит в несколько этапов:
• сосудистая воспалительная реакция - отек;
• формирование воспалительного экссудата;
• лизис утративших жизнеспособность тканей;
• запуск и стимуляция иммуноцитогенеза.
В результате очаг травматической деструкции (рана), пополняясь клеточными популяциями за счет мигрирующих фагоцитов, лимфоцитов, тромбоцитов, эндотелиоцитов, фрагментами мертвых тканей и элементами первичного загрязнения, преобразуется в очаг нагноения - гнойную рану. Это заменяет позитивный процесс самоочищения очага повреждения негативным воспалительно-деструктивным процессом с вовлечением в процесс живых тканей на границе очага травматической деструкции. Вследствие этого одной из наиболее сложных хирургических проблем является корректное лечение пациентов на различных этапах развития гнойных заболеваний.
По данным отечественных авторов, в общей структуре хирургических заболеваний хирургическая инфекция наблюдается у 35 - 45% больных [1]. Хирургические инфекции мягких тканей являются ведущей патологией в структуре первичной обращаемости хирургических больных на амбулаторно-поликлиническом этапе, а на стационарном - послеоперационные назокомиальные инфекции мягких тканей, которые по данным Шляпникова С.А., 2003 г. [2] занимают лидирующее место, составляя 40% всех госпитальных инфекций. Белобородов В.Б. и Джексенбаев О.Ш., 1991 г. [3], а также Белобородова Н.В. и Бачинская Е. Н., 2000 г. [4] показали, что инфекции в области хирургического вмешательства занимают ведущее место в структуре внутрибольничных инфекций и возникают примерно у 5 - 35 из 100 оперированных пациентов, и увеличивают срок пребывания в стационаре, в среднем, на 5 - 8 дней. Риск гибели таких больных в 2 раза выше, а вероятность повторной госпитализации в 5 раз выше по сравнению с пациентами без инфекции. Продолжительность пребывания пациента в стационаре, в связи с инфекцией в области хирургического вмешательства, увеличивается, в среднем, на 6,5 дней, а стоимость больничных расходов возрастает вдвое. Частота воспалительных осложнений после различных хирургических вмешательств находится в пределах от 9,0% до 37,8% [5]. Многие отечественные ученые [1,6] сходятся во мнении, что достижения современной науки позволяют расширить, а в некотором отношении и по-новому рассматривать многие представления о взаимоотношении микроорганизмов с человеком, вопросы этиопатогенеза, диагностики, лечения, оценки прогноза хирургических инфекционных заболеваний и их осложнений. Особая роль принадлежит внедрению в практику новых методов диагностической визуализации, малоинвазивной хирургической техники, успехам в разработке антимикробных и иммунокоррегирующих средств, методологии интенсивной поддерживающей терапии. Прогресс применения ультразвукового исследования (УЗИ) в гнойной хирургии, обусловлен улучшением применяемых компьютерных технологий и качеством преобразователя [7]. Данные, представленные в работах Евдокимовой Е.Ю., Жестовской С.И., 2000 г. [8] и Lavoipierre A.M., Kremer S., 1999 г. [9] свидетельствуют о том, что увеличенное пространственное и контрастное изображение через современные преобразователи, использование технологии отображения гармоники и лучшего цвета, методик допплеровского отображения, облегчают постановку диагноза.
Ультразвуковое исследование имеет ряд преимуществ перед другими методами. В частности, Loyer E.M., Kaur H., David C.L. et al. 1995 г. [10], Сажин В.П. с соавт., 2004 г. [11] и Sisley Amy C., Bonar J.P., 2005 г. [12] указывают на возможность динамического наблюдения за течением раневого процесса. Возможность контакта между специалистом и пациентом во время экспертизы, позволяют вести мониторинг лечения, обеспечивает возможность своевременной контролируемой пункции исследуемого объекта для введения лекарственных препаратов или забора материла для исследования [13,14]. УЗИ не требует много времени для выполнения и не имеет побочных эффектов, что подчеркивает перспективность этого метода [15]. Newman J.S. etal. 1994 г. [16] сообщают, что современные допплеровские методики обеспечивают возможность оценки сосудистой реакции в зоне обнаруженных изменений, при этом чувствительность метода достигает 93% [17]. По данным Latifi H.R. et al. 1994 г. [18]; Rubin J.M., 1999 г. [19] чувствительность и специфичность метода составляет 79% и 62% соответственно.
Волчанский А.И., 1998 г. [20], Жестовская С.И., 2003 г. [21 ], Измайлов С.Г. с соавт., 2003 г. [5], Бор-даков В.Н., Абрамов Н.А., 2004 г. [22] и Чебышева Э.Н., 2005 г. [23] считают, что изучение динамики послеоперационных изменений в зоне оперативного вмешательства с помощью УЗИ позволяет на ранних стадиях определять не проявляющиеся клинически послеоперационные осложнения (инфильтраты, жидкостные скопления) до развития гнойного процесса. Абсцессы и инфильтраты передней брюшной стенки являются осложнением ряда заболеваний, повреждений и оперативных вмешательств на органах брюшной полости, забрюшинного пространства и таза [24]. Данные Биссет Р.А. и Хан А.Н., 2003 г. [25] свидетельствуют о широком использовании ультразвукового исследования в диагностике абсцессов мягких тканей передней брюшной стенки. Так, Евдокимова Е.Ю., 2003 г. [26], основываясь на результатах обследования и лечения 202 пациентов, показала, что ультразвуковой метод обладает высокой эффективностью для выявления послеоперационных гнойных и воспалитель-но-инфильтративных осложнений заболеваний брюшной полости и забрюшинного пространства: чувствительность - 97,8%, специфичность -89,5%, точность - 97,1%.
По мнению Robert Hill M.D. и Richard Conron D.O., 1997 г. [27] УЗИ имеет приоритетное значение при возникновении воспалительного процесса, связанного с наличием инородного тела в мягких тканях. Под инородным телом в данном случае рассматриваются разного рода трансплантаты и протезы, установленные с медицинской целью. Ультразвуковыми критериями гнойного поражения парапротезных тканей, согласно исследованию Цветкова В.О., 2003 г. [28], является наличие характерных изменений структуры мягких тканей - понижение их эхоплотности с нарушением нормальной анатомической структуры, а также наличие в мягких тканях зоны повышенной эхоплотности с неоднородными гипоэхогенными включениями, а так же газовых включений. Важное значение приобрело ультразвуковое исследование в диагностике парапротезной инфекции после реконструктивных операций на кровеносных сосудах. УЗИ дает возможность определения точной локализации воспалительного очага, отношение его к сосудистому протезу, глубину залегания и диаметр сосуда, определение параметров кровотока по протезу [28]. В своей работе автор приводит данные об эффективности УЗИ в диагностике парапротезной инфекции у больных после протезирования сосудов: при инфильтративных изменениях мягких тканей чувствительность- 64,0%, специфичность - 100%; при скоплении жидкости вокруг протеза чувствительность - 85,3%, специфичность - 100%. Г.И. Кунцевич с соавт., 1999 г. [29] доказана необходимость динамического наблюдения за больными после реконструктивных сосудистых операций с помощью УЗ-методов исследования, обеспечивающих выявление ранних нарушений регионарной гемодинамики задолго до момента клинических проявлений прогрессирования заболевания или развития осложнений, особенно при подозрении на развитие парапротезной инфекции. Таким образом, для адекватного заживления послеоперационной раны следует проводить мониторирование состояния мягких тканей пациента для выявления патологических изменений (жидкостных скоплений, воспалительных инфильтратов ит.д.), а также для динамической оценки состояния этих изменений с целью предотвращения инфицирования.
УЗИ, наряду с высокой точностью в диагностике воспалительных изменений мягких тканей, имеет и другие преимущества перед альтернативными методами визуализации: оно не несет лучевой нагрузки на пациента и врача, позволяет контролировать объект интереса и процесс внедрения иглы при пункции в реальном масштабе времени, сохраняет контакт врача и пациента. УЗ-исследование наиболее комфортно для больного. Мобильность ультразвуковых аппаратов дает возможность использовать их в условиях операционной или реанимационной палаты, при невозможности транспортировки больного, например при проведении искусственной вентиляции легких. При УЗ-исследовании для изучения поверхностно расположенных тканей используют датчик с частотой 7,5 МГц; более глубокие структуры области плеча, бедра, ягодичные области, а также переднюю брюшную стенку при наличии выраженной гипертрофии жирового слоя обследуют датчиками с частотой 5,0 и/или 3,5 МГц. В норме кожа в ультразвуковом изображении представляется однородной эхогенной полоской толщиной от 2,0 до 6,0 мм. Подкожная жировая клетчатка вариабельна по толщине, выглядит в виде слоя умеренной эхогенности с сетчатой структурой фиброзной стромы. Подкожные сосуды в норме, как правило, не выявляются. Тонкая (1-2 мм) эхогенная поверхностная фасция повторяет контур мышечного слоя, от которого она отделена прослойкой субфасциального жира. В мышечном слое отчетливо дифференцируются отдельные мышцы, имеющие пониженную эхогенность и характерную структуру (перистую в продольном - и сотовидную в поперечном сечении). Мышечные жировые прослойки отличаются повышенной эхогенностью при сравнении с тканью мышцы.
Цель исследования
Динамическое УЗ - наблюдение за состоянием мягких тканей в области послеоперационной раны для определения рациональной тактики ведения пациента в послеоперационном периоде.
Материалы и методы
Обследовано 165 пациентов после перенесенных оперативных вмешательств, которые были разделены натри группы:
I-128 (77,6%) пациентов после оперативного вмешательства по поводу хирургической патологии органов брюшной полости и забрюшинного пространства;
II-12 (7,3%) пациентов после грыжесечения с комбинированной пластикой сетчатым эндоп-ротезом (Surgpro-mesh);
III - 25 (15,1%) пациентов после аллопротези-рования аорты, магистральных артерий нижних конечностей, шеи.
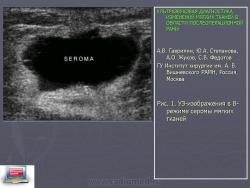
Рис. 1. УЗ-изображения в В-режиме серомы мягких тканей
Всем пациентам после оперативного вмешательства проведено УЗИ мягких тканей брюшной стенки, нижних конечностей и шеи в В-режиме с целью выявления патологических изменений, с определением размеров, структуры и указанием локализации относительно поверхности кожи; в 5 наблюдениях при подозрении на наличие инфицирования процесса проводили дуплексное сканирование мягких тканей вокруг выявленного очага; при выявлении патологических изменений вокруг сосуда или протеза после протезирования магистральных сосудов выполняли дуплексное сканирование для определения гемодинамической ситуации в сосуде или протезе.
Результаты исследования
Клиническая картина у данного контингента больных была вариабельна: в 56 (33,9%) наблюдений пациенты жаловались на повышение температуры, в 67 (40,6%) - на наличие болевых ощущений в области послеоперационной раны, также могло отмечаться покраснение кожи, у 14 (8,5%) пациентов отмечалось сочетание повышения температуры с наличием болевых ощущений и покраснением кожных покровов в области послеоперационной раны; в 40 (24,2%) случаях пациенты не предъявляли особых жалоб. При наличии жалоб и/или клинических проявлений ультразвуковое исследование мягких тканей проводилось сразу же при их появлении, при отсутствии жалоб - на третьи, шестые и девятые сутки после оперативного вмешательства.
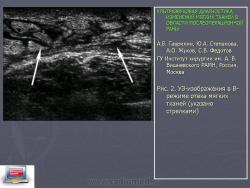
Рис. 2. УЗ-изображения в В-режиме отёка мягких тканей (указано стрелками)
В I группевыявлены ограниченные жидкостные скопления различной формы, размеры которых варьировали от 7,0- 8,0 мм до 50,0 мм в диаметре и от 10,0 - 15,0 мм до 150,0 - 180,0 мм по протяженности. По структуре в 32 (25,0%) наблюдений диагностированы анэхогенные и гипоэхогенные (однородные и неоднородные) жидкостные скопления (Рис. 1); в 19 (14,8%) случаях выявлены инфильтративно-воспалительные изменения тканей. В 9 (7,0%) наблюдениях имело место сочетание жидкостного скопления и инфильтративно-воспалительных изменений окружающих тканей.
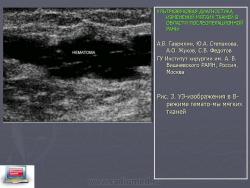
Рис. 3. УЗ-изображения в В-режиме гематомы мягких тканей
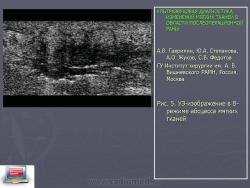
В 13 (10,2%) наблюдениях выявлен отек мягких тканей (Рис. 2), определяемый локальной пониженной эхогенности мягких тканей с неровными нечеткими контурами и незначительно выраженными узкими жидкостными «ходами» (толщиной до 0,9 мм) между мышечными волокнами и жировыми дольками. Гематома мягких тканей (Рис. 3), определяемая как моно- или полициклическое образование с четкими или нечеткими ровными контурами, по структуре гипоэхогенное неоднородное, ячеистой структуры, диагностирована в 25 (19,5%) наблюдениях. В 44 (34,4%) наблюдениях выявлен инфильтрат мягких тканей в виде зоны с нечеткими неровными контурами, по структуре гипо- и изоэхогенной неоднородной (Рис. 4). Также, в 15 (11,7%) случаях визуализировались образования с нечеткими неровными контурами, чаще неправильной формы, по структуре неоднородное, пониженной эхогенности с наличием анэхогенных зон и гиперэхогенных включений, дающих и не дающих акустическую тень, вокруг которого определялся эхоплотный валик, что при соответствующей клинической картине указывало на картину абсцесса (Рис. 5). В 12 (9,4%) наблюдениях патологические изменения, выявленные в мягких тканях, четко не дифференцировались от окружающих тканей, определялись в виде узких жидкостных «ходов» меж мышечных волокон, эхоструктура мягких тканей при этом была уплотнена и несколько «смазана» с наличием единичных мелких гиперэхогенных включений. Клинически эти УЗ-признаки сопровождались гектическим повышением температуры и были в дальнейшем верифицированы как флегмона.
В 12 (9,4%) наблюдениях определено увеличение регионарных лимфатических узлов.
Рис. 4.УЗ-изображения в В-режиме инфильтрата мягких тканей (указано стрелками)
Рис. 5. УЗ-изображение в В-режиме абсцесса мягких тканей
Во II группепациентов во всех наблюдениях визуализировался сетчатый эндопротез в виде гиперэхогенной линейной структуры. Ограниченные жидкостных скопления диагностированы в 9 (75,0%) случаях, как правило, они имели вытянутую форму и локализовались как над, так и под протезом, их размеры варьировали от 10,0 мм до 68,0 мм в диаметре, протяженностью от 12,0 мм до 170,0 мм. Структура жидкостных образований была преимущественно анэхогенная диффузно неоднородная (Рис. 6). В 7 (28,0%) наблюдениях жидкостное скопление сопровождалось наличием инфильтратив-но-воспалительных изменений. В 1 (4,0%) случае отмечали выраженный отек мягких тканей в виде узких жидкостных полосок (толщиной до 1,0 - 1,3 мм) между мышечными волокнами и жировыми дольками. В 1 (8,3%) наблюдении диагностировано наличие гематомы. И в 1 (8,3%) - образование с нечеткими неровными контурами, неправильной формы, по структуре неоднородное, пониженной эхогенности с наличием анэхогенных зон и гиперэхогенных включений, дающих и не дающих акустическую тень, расцененное, как абсцесс.
В 1 (8,3%) наблюдении определено увеличение регионарных лимфатических узлов.
Рис. 6. УЗ-изображения в В-режиме жидкостного скопления в мягких тканях (указано стрелками) по ходу сетчатого эндопротеза (S- эндопротез)
Рис. 7. УЗ-изображения в режиме ЭОДС жидкостного скопления муфтообразно охватывающего протез (указано стрелками)
В III группепациентов диагностированы жидкостные скопления размером от 10,0 мм до 67,0 мм в диаметре и от 10,0 - 15,0 мм до 180,0 - 215,0 по протяженности. В 7 (28,0%) случаях диагностированы жидкостные скопления, муфтообразно охватывающие протез, скопления имели четкие ровные контуры, ан- и гипоэхогенную неоднородную структуру (Рис. 7). В 5 (20,0%) наблюдениях в мягких тканях диагностированы жидкостные анэхогенные и гипоэхогенные (однородные и неоднородные) по структуре скопления незначительных размеров, не контактирующие непосредственно с протезом (Рис. 8). В 2 (8,0%) случаях выявлено сочетание жидкостного скопления и инфильтративно-воспали-тельных изменений окружающих тканей, представленные, как правило, инфильтратом с нечеткими неровными контурами, по структуре изоэхогенным неоднородным с наличием жидкостного скопления или жидкостных «ходов» неправильной формы. В 14 (56,0%) наблюдениях выявлены гематомы, располагавшиеся по ходу протеза/сосуда (Рис. 9) или охватывающие протез на различную величину по окружности, представленные гипоэхо-генными неоднородными образованиями, с четкими неровными контурами, ячеистой структуры, размеры которых варьировали от 30,0 мм до 140,0 мм. Инфильтрат мягких тканей, определяемый как зона с нечеткими неровными контурами, по структуре гипо-и изоэхогенная неоднородная с наличием в 1 случае мелких анэхогенных включений, диагностирован в 2 (8,0%) наблюдениях. В 4 (16,0%) наблюдениях диагностированы патологические изменения мягких тканей с плохо дифференцируемыми границами в виде узких жидкостных «ходов» меж мышечных волокон, структура мягких тканей при этом уплотнена и несколько «смазана», отмечали наличие единичных мелких гиперэхогенных включений, расцененные, учитывая клинические данные, как флегмона.
Рис. 8.Изображение в режиме Sie-Scapeжидкостного скопления в мягких тканях по ходу сосуда
У 5 пациентов III группы, при наличии выраженных инфильтративно-воспалительных изменений в мягких тканях по ходу послеоперационного шва с наличием жидкостного компонента, проведенное дуплексное сканирование выявило усиление сосудистого рисунка вокруг области инфильтрации. Дуплексное сканирование сосудов после протезирования в 1 (4,0%) наблюдении диагностировало тромбоз протеза (Рис. 10), просвет которого в режиме ЦДК и ЭОДС не окрашивался, кровоток не регистрировался. В остальных наблюдениях визуализировалось равномерное окрашивание просвета сосуда или протеза, а также отсутствие локальных изменений скорости кровотока. В 5 (25,0%) наблюдениях визуализированы увеличенные регионарные лимфатические узлы. Пациентам с выявленными патологическими изменениями мягких тканей проводилось динамическое ультразвуковое мониториро-вание состояния области оперативного вмешательства, которое выявило следующие результаты.
У 11 (23,9%) пациентов, при выявлении жидкостных скоплений значительных размеров, проводились лечебно-диагностические пункции под УЗ-контролем с целью эвакуации жидкостного содержимого и лабораторного исследования пунктатов: I группа - 5 наблюдений, II группа - 2 наблюдений, III группа - 4 наблюдений. Данные цитологического исследования свидетельствовали о наличии сером, иногда с присутствием элементов крови.
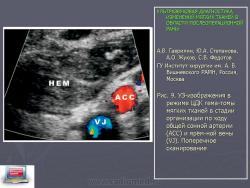
Рис. 9.УЗ-изображения в режиме ЦДК гематомы мягких тканей в стадии организации по ходу общей сонной артерии (АСС) и ярёмной вены (VJ). Поперечное сканирование
В остальных 35 (76,1%) случаях проводилось динамическое УЗ-мониторирование жидкостных скоплений. При динамическом УЗИ в 7 (20,0%) случаях, при наличии клинических проявлений, на фоне приема антибиотиков, а также при увеличении размеров скопления или длительном отсутствии положительной динамики, проводились лечебно-диагностические пункции в отсроченном периоде: I группа - 4 наблюдений, II группа - 2 наблюдений, III группа -1 наблюдение У остальных 28 (80,0%) пациентов отмечалась положительная динамика (I группа - 23 наблюдений, II группа - 5 наблюдений), не требующая выполнения инвазивных вмешательств.
При наличии инфильтративных изменений мягких тканей во всех наблюдениях, вследствие отсутствия клинических проявлений проводилось динамическое наблюдение, которое констатировало их регресс.
Диагностированный отек мягких тканей во всех 14 наблюдениях регрессировал при динамическом наблюдении.
В случае выявления гематом мягких тканей в 22 (55,0%) наблюдениях при незначительных размерах (размерами до 50,0 мм) проводилось динамическое УЗ-наблюдение гематомы до ее организации. При значительных размерах гематомы (наибольшие размеры составили 140,0х46,0 мм), а также при наличии при этом субфебрильной температуры, проводилось чрескожное пункцион-ное лечение под УЗ-контролем: в I группе в 12 наблюдениях, во II группе - в 1 и в III группе -в 2 случаях. В 3 случаях (в III группе больных) при наличии гематомы, окутывающей протез,выполнено оперативное вмешательство с эвакуацией плотного компонента диагностированных гематом.
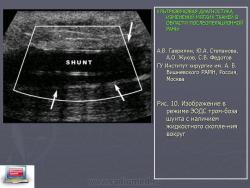
Рис. 10.Изображение в режиме ЭОДС тромбоза шунта с наличием жидкостного скопления вокруг
Инфильтрат мягких тканей, диагностированный в 33 наблюдениях (в I группе - 31 наблюдение, в III группе - 2 наблюдения), не потребовал хирургических вмешательств, так как данные УЗ-мониторирования свидетельствовали о постепенном регрессе патологического процесса.
При выявлении абсцесса мягких тканей в 3 (18,7%) наблюдениях пациентов I группы проводилось чрескожное пункционное лечение под УЗ-контролем, в 13 (81,3%) случаях (в I группе -12 наблюдений, во II - 1 наблюдение) значительные размеры абсцесса и/или наличии клинических проявлений (повышение температуры тела до 39°С и выраженный болевой синдром в области послеоперационной раны) явились показанием к выполнению оперативного вмешательства.
Во всех 16 наблюдениях при выявлении флегмоны проводилось оперативное вмешательство с целью санации и дренирования мягких тканей в области оперативного вмешательства.
При тромбозе протеза, диагностированном при дуплексном сканировании у пациента III группы, выполнялось оперативное вмешательство, восстановившее кровоток.
Обсуждение
Данные проведенного исследования свидетельствуют о некоторой специфике послеоперационных изменений, характерной для различных оперативных вмешательств, так для пациентов I группы, перенесших оперативное вмешательство по поводу хирургических патологий органов брюшной полости и забрюшинного пространства, характерно наличие гнойно-воспалительных изменений (45,3%); для пациентов II группы, после грыжесечения с комбинированной пластикой сетчатым эндопротезом (Surgpro-mesh), характерно наличие сером (75,0%); в III группе пациентов, после протезирования аорты, магистральных артерий нижних конечностей, шеи чаще выявляли гематомы (56,0%). Также можно отметить, что после различных оперативных вмешательств УЗ-картина сером, инфильтратов и отека имеет некоторые отличия. Результаты ультразвукового динамического наблюдения за состоянием мягких тканей у пациентов, перенесших оперативное вмешательство, показали, что эти данные сопоставимы с аналогичными, полученными Волчанским А.И., Жестовской С.И., Измайловой С.Г с соавт., Бордаковым с соавт., Абрамовым Н.А. и Чебышевой Э.Н. УЗИ позволяет с минимальными затратами и без ионизирующей лучевой нагрузки выявлять послеоперационные осложнения в виде жидкостных скоплений и инфильтратов, не имеющих клинические проявления. Особое место занимает выявление гнойно-воспалительных изменений (абсцессов, флегмон). Наши данные соответствуют результатам, полученным Биссет Р.А. и Хан А.Н., и дают возможность вовремя выявить эти осложнения и предотвратить распространение и генерализацию процесса. Несомненно, важным является мониторирование мягких тканей передней брюшной стенки у пациентов после грыжесечения с комбинированной пластикой сетчатым эндопротезом. Вследствие того, что в нашем исследовании пациенты этой группы преимущественно имели повышенную массу тела, а в 3 (25,0%) случаев сахарный диабет в качестве сопутствующего заболевания, заживление раны происходило с повышенным риском гнойных послеоперационных осложнений, в условиях наличия инородного тела (протеза). Выявленные изменения соответствуют данным, представленным в исследованиях Robert Hill M.D. и Richard Con-ron D.O., а также Цветкова В.О. Реконструктивные операции на магистральных сосудах брюшной полости широко выполняются в хирургических клиниках. Возраст пациентов, сопутствующие заболевания и обменные нарушения нередко приводят к возникновению послеоперационных гнойных осложнений в мягких тканях, а также к нарушению кровотока по реконструированным сосудам. Ультразвуковое исследование является в этом случае методом выбора для наблюдения пациентов в послеоперационном периоде, так как оно позволяет не только выявить патологические изменения в мягких тканях, но и диагностировать пристеночные и окклюзирующие изменения в просвете сосуда или протеза. Результаты нашего исследования подтверждают мнение Цветкова В.О. и Кунцевич Г.И. о необходимости динамического УЗ-мониторирования пациентов данной категории после оперативного вмешательства. Таким образом, ультразвуковой мониторинг состояния мягких тканей в области послеоперационной раны позволяет диагностировать жидкостные скопления, гематомы и инфильтративно-воспалительные изменения в зоне оперативного вмешательства. Это дает возможность хирургам определить тактику рационального ведения больного и уменьшить риск гнойных осложнений в области послеоперационной раны.
Список литературы
1. Федоров В.Д., Светухин А.М. Стратегия и тактика лечения обширных гнойных ран. Избранный курс лекций по гнойной хирургии. М., Миклош. 2003; 18-30.
2. Шляпников С.А. Хирургические инфекции мягких тканей - старая проблема в новом свете. Инфекции в хирургии. 2003; 1(1): 14 - 21.
3. Белобородов В.Б., Джексенбаев О.Ш. Эндотоксины грамотрицательных бактерий. Цитокины и концепция септического шока; современное состояние проблемы. Анестезия и реаниматология. М.,1991; 4:41 -43.
4. Белобородова Н.В., Бачинская Е.Н. Иммунологические аспекты послеоперационного сепсиса. Анестезия и реаниматология. 2000; 1: 59 - 66.
5. Измайлов С.Г., Измайлов Г.А., Тюдушкина И.В. и др. Лечение ран. - Казань: изд-во Казанского государственного технического университета. 2003; 137 - 144.
6. Ерюхин И.А., Гельфанд Б.Р., Шляпников С.А. Хирургические инфекции: руководство. С-Пб.: издательский дом «Питер» (Серия «Спутник врача»), 2003; 864.
7. HedrickWR, HykesL, StarchmanDE. Static imaging principles and instrumentation. In: Ultrasoundphysicsandinstrumentation. StLouis(MO): Mosby.1995; 71 -87.
8. Евдокимова Е.Ю., Жестовская С.И. Роль ЦДК в диагностике стадий раневого процесса мягких тканей у больных с хирургической патологией Материалы краев. науч.-практ. конференции, посвященной 50-летию общества рентгенологов и радиологов. Красноярск. 2000; 37 - 38.
9. Lavoipierre AM, Kremer S. Cabrini Hospital, Melbourne The expanding role of ultrasound in medicine. Aust. Fam. Physician. 1999; 28 (11): 1121 - 7.
10. Loyer E.M., Kaur H., David C.L., DuBrow R. et al.Importance of dynamic assessment of the soft tissuesin the sonographic diagnosis of echogenic superficial abscesses. Department of Diagnostic Radiology,University of Texas M.D. Anderson Cancer Center, Houston 77030, USA. Journal of Ultrasound inMedicine. 1995; 14(9): 669 - 671.
11. Сажин В.П., Жаболенко В.П., Авдовенко А.Л. и др.Роль сонографии в оценке течения раневого процесса у больных после эндовидеохирургического лечения постинъекционных абсцессов ягодиц. Институт хирургии им. А. В. Вишневского РАМН. Материалы конференции, посвященной 10-летию отделения ультразвуковой диагностики.