Рентгенодиагностика диффузных и диссеминированных заболеваний легких.
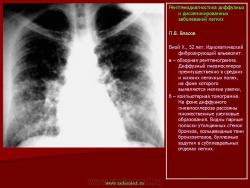
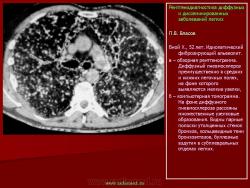
Ведущими клиническими симптомами ИФА являются кашель, прогрессирующая одышка. При мерно у половины больных наблюдаeтся деформация фаланг по типу барабанных палочек. При пневмосклерозе происходит уменьшение эластического резерва легочной ткани. Ригидность соединительнотканной стромы ведет к ограничению растяжимости легкого и, соответственно, к уменьшению альвеолярной вентиляции. Повреждение альвеоло-капиллярных мембран затрудняет газообмен между альвеолами и капиллярами, страдает оксигенация артериальной крови. В результате развивается респираторная, а затем и сердечная недостаточность, которая, в конечном счете, ведет к летальному исходу. Для фиброзирующего альвеолита характерно быстрое развитие легочно-сердечной недостаточности, которая часто приводит к летальному исходу в течение нескольких месяцев (М.М. Илькович с соавт. 1984, 1998; Н.В. Путов и М.М. Илькович, 1986; S.M. Ellis и D.M. Hansel, 2002; S.L. Primack с соавт. ,1993). В ряде случаев при ретроспективном анализе рентгенограмм можно отметить изменения рентгенологической картины за несколько лет до появления первых клинических симптомов (I.D. Johnston с соавт., 1997; M. TurnerWarwick, 1980) [32, 33]. Вместе с тем, описаны случаи острого и даже молниеносно протекающего идиопатического фиброзирующего альвеолита (А.Г. Чучалин, 2000; M. Akira с соавт., 1997, 1999; T.E. Hartman с соавт., 2000; A.L. Katzenstein и R.F. Fiorelli, 1994; T.S. Kim с соавт., 1998; J.S. Parck с соавт., 1995; D.S. Pratt с соавт., 1979; S.L. Primack с соавт.
При идиопатическом фиброзирующем альвеолите на рентгенограммах обычно выявляется двустороннее симметричное усиление легочного рисунка. В противоположность саркоидозу, для которого характерно преобладание изменений в прикорневых отделах легких, при фиброзирующем альвеолите легочная ткань поражается более равномерно. Отмечено некоторое преобладание из менений в базальных и периферических, субплевральных отделах. Диффузная пролиферация фиброзной ткани ведет к деформации и перестройке архитектоники легочного рисунка по сетчатому типу. В периферических, субплевральных отделах легочный рисунок приобретает вид “пчелиных сот”, формируется картина так называемого “сотового легкого”: утолщенные межальвеолярные, периацинарные и междольковые перегородки охватывают эмфизематозно вздутые дольки и ацинусы. Для фиброзирующего альвеолита типичным является развитие буллезной эмфиземы, которая обычно развивается раньше других изменений легочного рисунка. Эмфизематозные буллы лопаются, вследствие чего иногда возникает спонтанный пневмоторакс, который может повторяться несколько раз. Одним из ранних рентгенологических проявлений идиопатического фиброзирующего альвеолита является диффузное понижение пневматизации типа матового стекла. C.Bergin с соавт. (1990) отметили, что при ИФА нередко наблюдается увеличение бронхопульмональных и медиастинальных лимфатических узлов. Следует однако иметь ввиду, что расширение корней легких при фиброзирующем альвеолите может быть вызвано увеличением калибра магистральных сосудов, вследствие гипертензии в малом круге кровообращения. Описанные признаки легочной гипертензии в далеко зашедшей стадии заболевания сочетаются с картиной так называемого легочного сердца. При фиброзирующем альвеолите вследствие уменьшения объема легких, диафрагма обычно занимает высокое положение. И.В. Васильчук (1985) отметила уменьшение объема легких и высокое положение диафрагмы с ограничением ее подвижности более чем у половины больных с идиопатическим фиброзирующим альвеолитом. Признаки легочной гипертензии отмечены у 30% больных. Нередко появляются дисковидные ателектазы. Функциональные исследования подтверждают наличие высокой степени респираторной недостаточности. Реография позволяет выявить признаки гипертензии малого круга кровообращения и дать ей количественную оценку. Сцинтиграфия может показать значительное понижение капиллярного кровотока, в местах наиболее выраженных изменений рентгенологической картины.
П.В. Власов
Кафедра лучевой диагностики Института повышения квалификации Федерального медикобиологического агентства
Диффузные интерстициальные и диссеминированные процессы легких представляют одну из сложнейших проблем клинической медицины с точки зрения диагностики и лечения. Широкое применение антибиотиков и других лекарственных средств, различного рода химических препаратов в промышленном производстве и повседневной жизни, биостимуляторов, дефолиантов, гербицидов и пестицидов существенно повлияло на иммунологический статус населения. Все это изменило структуру патологии, с которой приходится сталкиваться врачу в повседневной клинической практике. В структуре легочных болезней произошел заметный сдвиг в сторону заболеваний диффузного интерстициального характера не известного генеза. По данным различных консультативных центров, этот вид патологии составляет около 5% всех поражений легких. На нозологическую структуру диссеминированных процессов легких влияют особенности региональной патологии и специфика лечебного учреждения. Так, согласно исследованиям В.А. Соколова (1976), среди больных с диссеминированными процессами в легких наибольшую группу составили больные силикозом (32%), на туберкулез приходится 30%, на хронические неспецифические заболевания легких 6,2%, редкие болезни зарегистрированы у 5%. Данные В.А. Соколова отражают характер краевой патологии Уральского региона с развитой горнорудной промышленностью и специфику материала Уральского НИИ фтизиопульмонологии. По данным Узбекского НИИ фтизиатрии и пульмонологии, среди больных с диссеминированными процессами в легких доминирует туберкулез. В группе больных в количестве 180 человек с различными заболеваниями диффузного и диссеминированного характера были установлены следующие формы: диссеминированный туберкулез легких 500/0, НЗЛ – 19,4%, силикоз – 9,4%, карциноматоз – 7,2%), экзогенный аллергический альвеолит – 2,8%, идиопатический фиброзирующий альвеолит 2,2%, токсический фиброзирующий альвеолит – 0,6%, пневмокониоз – 3,9%, коллагеноз – 3,3%, лимфогранулематоз – 1,1% (М.В. Абдурашитова с соавт., 1989). По материалам кафедры легочного туберкулеза 1-го ЛМИ (З.И. Костина, 1984), среди довольно большой группы больных с диссеминированными процессами в легких (372 человека) на первом месте по частоте стоит саркоидоз (34,5%), на втором диссеминированный туберкулез (24,8%). Пневмокониозы составили 7,5%. Согласно данным Н.Б. Буровой с соавт. (1984), основанным на материале Московской клинической больницы № 1, охватывающем 211 больных с диссеминированными процессами легких, нетуберкулезные заболевания выявлены у 180 (85,3%). Среди них наибольшую группу (63,5%) составили больные саркоидозом. Редкие заболевания (альвеолярный протеиноз, болезнь ХаменаРича, фиброзирующий альвеолит и проч.) в этой группе больных составили 6,7%. По мнению М.М. Ильковича и Л.Н. Новиковой (1998), на интерстициальные пневмопатии приходится 20% всех болезней легких. Интерстициальные болезни легких представляют собой гетерогенную группу, объединяемую общими клиническими проявлениями, изменениями физиологии дыхания и определенным рентгеноморфологическим сходством (А.Г. Чучалин, 2000; J.D. Fulmer, 1982). Многие авторы сходятся на том, что большинство интерстициальных болезней имеют разную этиологию, но общий патогенез (А.Г. Чучалин, 2000; R.G. Crystal с соавт., 1981; J.D. Fulmer, 1982). В некоторых случаях пусковым механизмом являются экзогенные токсические факторы, непосредственно поражающие альвеолярные клетки или клетки эндотелия капилляров. Органические пыли и некоторые лекарства действуют на легкие через иммунные механизмы. Подсчитано, что число нозологических форм, сопровождающихся диффузными интерстициальными и узелковыми процессами в легких превышает 150 наименований (С.А. Рейнберг, 1962; C.P. Carrington и E.A. Gaesner, 1978; T.C. McLoud с соавт., 1983), однако в клинической практике 90% подобных состояний приходится на 8–10 наиболее распространенных заболеваний. Все подобные заболевания условно можно разделить на две группы. В первую группу входят заболевания, преобладающим морфологическим признаком которых является наличие гранулем, определяющих клинико-морфологическую сущность каждой гранулематозной болезни.
Вторую группу интерстициальных заболеваний составляют поражения легких, характеризующиеся диффузными, преимущественно интерстициальными изменениями легочной ткани без формирования гранулем. Недостаточное знакомство врачей общей практики с клинико-рентгенологическими проявления заболеваний, сопровождающимися диффузным фиброзом и узелковой диссеминацией является причиной частых диагностических ошибок. М.М. Илькович и Л.Н. Новикова (1998) отмечают, что диагностические ошибки в группе больных с интерстициальными заболеваниями легких составляют 75–80%. По мнению авторов, в каждом втором случае интерстицильных пневмопатий природа легочной патологии остается не выясненной. По крайней мере, 50–70% больным с диффузными и диссеминированными поражениями легких первоначально ставится ошибочный диагноз туберкулеза легких, следствием чего является необоснованная противотуберкулезная химиотерапия (С.Е. Борисов, 1987; М.М. Илькович и Л.Н. Новикова, 1998; А.Г. Хоменко с соавт., 1991; Е.И. Шмелев, 2001). Эти разнообразные по патогенезу процессы сопровождаются сходными клиническими и рентгенологическими проявлениями, в связи с чем объединяются общим методологическим подходом к диагностике.
Методы исследования
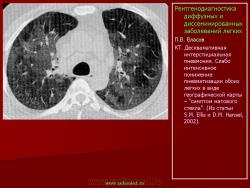
В диагностике диффузных и диссеминированных процессов ведущую роль принадлежит рентгенологическому исследованию органов грудной клетки, которое начинается с обзорной рентгенографии. К сожалению, на обзорных рентгенограммах грудной клетки мы получаем скиалогическую картину, которая является результатом суммации тенеобразований трехмерного объекта на плоскость. Вследствие эффекта суперпозиции и субтракции на плоскости получается картина, малопохожая на изображение каждого патологического образования в отдельности. Многие очаги сливаются и уходят в фон, вместе с тем появляются новые тенеобразования, для которых нет конкретного морфологического субстрата, то есть, которых нет на самом деле. При диффузных интерстициальных процессах и очаговой диссеминации неоднородная рассеивающая среда нивелирует нормальные элементы легочного рисунка, а именно сосуды среднего и малого калибра. Линейная томография при диффузном пневмосклерозе и мелкой диссеминации мало эффективна: мелкие очажки и линейные анатомические структуры, вследствие меньшей разрешающей способности линейной томографии, на рентгенограммах не выявляются. Проблему проекционного и суммационного искажения с успехом решает рентгенокомпьютерная томография (РКТ), особенно КТ тонкими срезами – так называемая высокого разрешения компьютерная томография (ВРКТ), которая благодаря высокой чувствительности детекторной системы, и соответственно способности охвата широкого спектра слабых плотностей, а также в силу исключения эффекта проекционной суммации позволяет выявлять детали, недоступные обычному традиционному рентгенологическому исследованию. На КТ чаще и более отчетливо выявляются тонкие структурные изменения, такие как сотовое легкое, лучше выявляются участки буллезной эмфиземы. Компьютерная томография позволяет оценивать состояние легочной ткани, перекрываемой массивными инфильтратами, выраженным фиброзом легочной ткани, значительным плевральным выпотом и массивными плевральными наслоениями. Причем, чем выше разрешающая способность КТ, тем точнее и реальнее отображаются узелковые и тяжистые структуры. Cовременные компьютерные томографы с программой высокого разрешения (ВРКТ) обладают заметными преимуществами перед обычными рентгенограммами, линейной томографией и даже компьютерной томографией толстыми срезами в выявлении мелких узелковых образований в интерстиции и паренхиме легкого, линейных и сетчатых структур. На ВРКТ выявляются мелкие узелковые образования диаметром около 2 мм, тонкие изменения интерстициального легочного рисунка, нормальные и патологически измененные сосуды и бронхи, хорошо выявляется тонкая сетка изменений междольковых и внутридольковых перегородок. С помощью ВРКТ открыт ряд новых рентгенологических симптомов, таких как симптом матового стекла, симптом булыжной мостовой, намного чаще стало выявляться сотовое легкое. Несмотря на сходство рентгенологической картины широкого круга заболеваний, сопровождающихся диффузным усилением интерстициального легочного рисунка, многие заболевания этой группы имеют определенную специфику, присущую каждому из них, которая позволяет приблизиться к единственно правильному диагнозу.
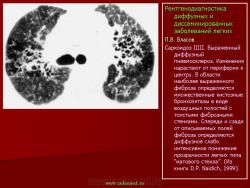
Саркоидоз
Саркоидоз является системным заболеванием неясного генеза, в основе которого лежит доброкачественный сходный с туберкулезом эпителиоидноклеточный гранулематоз. В отличие от туберкулеза в саркоидозных гранулемах обычно отсутствует казеозный некроз. Саркоидоз поражает преимущественно женщин в возрасте 30–40 лет. Чаще всего болезнь протекает доброкачественно на протяжении многих лет. По данным М.М. Ильковича (1989), бессимптомное течение наблюдается в 90–93% случаев саркоидоза. У части больных имеет место субфебрильная температура, повышенная утомляемость, боль в груди. Течение болезни волнообразное: обострения чередуются с ремиссиями. Реже болезнь протекает остро.
Хроническая форма саркоидоза на ранних стадиях болезни обычно протекает без каких-либо клинических проявлений. Общее самочувствие больного обычно не страдает. Иногда больные предъявляют жалобы на сухой кашель со скудным выделением мокроты. Лабораторные исследования также не дают надежных критериев для диагностики. При саркоидозе могут быть поражены все органы и ткани, но чаще встречается легочно-медиастинальная форма. Поражение органов дыхания встречается у 90% больных саркоидозом. В большинстве случаев диагноз саркоидоза органов дыхания ставится без особого труда.
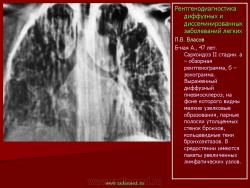
Рентгенологическая картина саркоидоза зависит от стадии процесса. Согласно классификации, предложенной R. Wurm (1960), получившей признание в нашей стране, различают три стадии саркоидоза: I – увеличение внутригрудных лимфатических узлов, II – развитие различных изменений легких (IIа – избыточный, петлистый рисунок в прикорневых и нижних отделах легких, IIb – образование мелких очагов милиарного типа, IIc – появление более крупных очагов размером 3–5 мм, IId – формирование очагов еще более крупных размеров до 6–9 мм и более), III – наличие выраженного фиброза и крупных конгломератных образований (IIIa – в нижних отделах, IIIb – в верхних и средних отделах легких) (А.И. Рабухин с соавт., 1975; А.Г. Хоменко с соавт., 1999).
На ранних стадиях развития саркоидоза при рентгенологическом исследовании выявляется увеличение различных групп лимфатических узлов. Наиболее характерным является симметричное увеличение бронхопульмональных и медиастинальных лимфатических узлов. А.И. Рабухин с соавт. (1975) среди большой группы исследованных больных саркоидозом ни у одного из них не обнаружили односторонней гиперплазии лимфатических узлов. Вместе с тем другие авторы отмечают, что примерно в 5–8% случаев встречается одностороннее увеличение лимфатических узлов средостения. В отличие от лимфогранулематоза не наблюдается изолированного увеличения паратрахеальных лимфоузлов. Легочный рисунок в этой стадии заболевания, как правило, сохраняет нормальную структуру. Иногда в прикорневых отделах он становится из быточным, в результате лимфостаза или начинающегося фиброза. В редких случаях в результате сдавливания бронхов увеличенными лимфоузлами возникает ателектаз легкого, чаще это касается средней доли.
Дифференциально диагностические трудности возникают главным образом во II стадии заболевания, когда происходит генерализация процесса с распространенным поражением легких интерстициального и узелкового характера. Диффузные формы саркоидоза, по данным З.И. Костиной (1989), составляют 6% среди всех больных с саркоидозом органов дыхания. На этой стадии заболевание чаще всего принимают за гематогенно-диссеминированный туберкулез. Согласно данным А.Е. Рабухина с соавт. (1975), примерно
у 20% больных на этой стадии происходит редукция увеличенных бронхопульмональных и медиастинальных лимфатических узлов. Поражение легких, повидимому, носит лимфогематогенный характер. В легких изменения характеризуются сочетанием интерстициальных изменений с очаговыми; последние обычно проявляются в виде диссеминации различной степени выраженности, появлением множественных гранулематозных узелков эпителиоидного характера, размерами от 2–3 до 10 мм. На компьютерных томограммах узелки, выделенные из общего интерстициального фона, имеют четкие контуры и однородную структуру. С прогрессированием болезни гранулемы постепенно замещаются фиброзной тканью. Согласно A.E. Voloudaki с соавт. (1999), для саркоидоза в компьютернотомографическом изображении характерно преобладание узелковых образований в периферических отделах легких, утолщение междольковых перегородок и уплотнение междолевой плевры. M.W. Brauner c соавт. (1989) обследовали с помощью высокоразрешающей компьютерной томографии 44 больных саркоидозом. Узелковые образования в легких были обнаружены у 25 больных. У 19 из них узелки были единственным проявлением легочного саркоидоза. У остальных они сочетались с другими изменениями. К прочим изменениям авторы относят сетчатые и линейные образования, утолщение плевральных листков, тракционные бронхоэктазы, воздушные полости. Изменения локализовались преимущественно в средних и верхних легочных полях задних отделов легких. Интерстициальные изменения при саркоидозе характеризуются диффузным, симметричным усилением и деформацией легочного рисунка, который приобретает груботрабекулярный, петлистый, крупноячеистый вид. На фоне полиморфной неравномерной разнокалиберной сетчатости видны грубые тяжистые структуры, веерообразно расходящиеся от корней легких к периферии. Фиброзные тяжи имеют неодинаковую толщину, преимущественно диаметром 3–5 мм. В отличие от диссеминированного туберкулеза, фиброзирующего альвеолита и гистиоцитоза, при саркоидозе формируется тяжистый фиброз по ходу крупных сосудисто-бронхиальных стволов. Изменения преобладают преимущественно в прикорневых, средних и верхних отделах легких. Корни легких обычно расширены и бесструктурны. Пневмосклероз сочетается с эмфиземой буллезного характера, которая больше выражена в кортикальных отделах легких.
В третьей стадии происходит слияние узелков в крупные конгломераты. Для саркоидоза II–III стадии типичным является несоответствие между степенью выраженности рентгенологических изменений легких и довольно скромной клинической симптоматикой. Тем не менее, с прогрессированием заболевания при нарастании фиброзных изменений в легких развивается респираторная недостаточность, причиной которой является нарушение растяжимости легкого, и нарушение диффузии кислорода – возникает альвеоло-капиллярный блок. Обширный фиброз легочной ткани с вторичной периацинарной эмфиземой может привести к развитию легочного сердца. Рентгенологическая картина саркоидоза во II–III стадии в какойто степени сходна с хроническим гематогенно-диссеминированным туберкулезом (А.Е. Рабухин, 1975; В.А. Соколов, 1987). В этих случаях следует учитывать различия в локализации процесса, наличие или отсутствие деструктивных изменений, характер очаговых изменений.
Идиопатический фиброзирующий альвеолит (синдром Хаммена-Рича)
Идиопатический фиброзирующий альвеолит (ИФА) впервые описали L. Hamman и A. Rich в 1944 г. на основании наблюдения четырех больных, умерших от непонятной интерстициальной пневмонии, сопровождавшейся прогрессирующей дыхательной недостаточностью, которая явилась причиной летального исхода. ИФА относится к группе прогрессирующих интерстициальных заболеваний легких, невыясненной природы. В основе заболевания лежат воспалительные изменения стенки альвеол, которые при прогрессировании заболевания заканчиваются интерстициальным фиброзом. Некоторые авторы относят это заболевание к коллагенозам – болезням соединительной ткани (системной красной волчанки, системной склеродермии, ревматоидного артрита, болезни Шегрена). Многие исследователи склонны считать идиопатический фиброзирующий альвеолит состоянием аутоиммуноагрессии с гиперэргической реакцией соединительной ткани. Учитывая сходство морфологических изменений в легких при идиопатическом фиброзирующем альвеолите, альвеолярном протеинозе и другими фиброзирующими процессами легких. М.М. Илькович и А.Н. Кокосов (1984) высказывают предположение, что фиброзирующий альвеолит является не нозологической формой, а фазой (стадией) патологических процессов разной этиологии. Сюда же авторы относят аллергические фиброзирующие альвеолиты. Во всяком случае, часть поражений стромы легких, объединяемых под названием “болезнь Хаммена–Рича”, по мнению авторов, является следствием аллергического альвеолита. В последнее время появилась тенденция относить фиброзирующий альвеолит к идиопатическим интерстициальным пневмониям (А.Г. Чучалин, 2000; S.M. Ellis и D.M. Hansel, 2002; T.E. Hartman с соавт., 2000; A.L. Katzenstein и R.F. Fiorelli, 1994; A.L Katzenstein и J.L. Myers, 1998; T.S. Kim с соавт., 1998; J.S. Parck с соавт., 1995; D.S. Pratt с соавт., 1979; S.L. Primack с соавт., 1993). Вместе с тем, тщательные бактериологические исследования не позволили выявить специфический характер возбудителя. Кроме того, морфологические изменения, присущие хроническому интерстициальному воспалению можно наблюдать при заболеваниях самой разнообразной, как установленной, так и неустановленной, этиологии и различного патогенеза (А.Г. Чучалин, 2000).



Системная красная волчанка
Системная красная волчанка большинством авторов относится к коллагенозам. Б. Визнер
(1984) описывает поражение легких при системной красной волчанке как воспалительное заболевание соединительной ткани. Болезнь характеризуется множественным поражением органов (кожи, слизистых оболочек, суставов, плевры, сердца, почек, лимфатических узлов, селезенки, печени, кроветворной системы, легких). Системной красной волчанкой страдают преимущественно молодые женщины, они составляют 80–90% всех заболевших. Наиболее частыми жалобами являются боли в грудной клетке, одышка, кашель, реже кровохарканье.
Для системной красной волчанки характерна стойкая лихорадка, резистентная к противоинфекционной терапии. Как правило, неосложненная лихорадка протекает с лейкопенией. Характерно высокое ускорение СОЭ, анемия и умеренная тромбоцитопения.
Морфологические изменения при этом заболевании неспецифичны и очень разнообразны.
Часто наблюдается умеренная полиадения – системное увеличение многих групп лимфатических узлов. Печень и селезенка также нередко увеличены. Обычно имеет место апластическое состояние костного мозга в целом или только лейко-тромбо- цитобластического, или эритробластического ростков. У подавляющего большинства больных в крови обнаруживаются волчаночные клетки.
На рентгенограммах органов грудной клетки определяется уменьшение объема легких и ограничение эластичности легочной ткани, диффузное усиление и деформация легочного рисунка, участки очагового или сегментарного понижения пневматизации, дисковидные ателектазы, высокое стояние диафрагмы и ограничение ее подвижности, наличие жидкости в плевральной полости.
Среди разнообразных легочных синдромов наиболее характерен волчаночный пневмонит. Это хронически протекающий воспалительный процесс с преимущественным вовлечением периваскулярной, перибронхиальной, междольковой соединительной ткани и альвеолярных перегородок (В. Насонова, 1966). Системная красная волчанка часто (в 57% случаев), осложняется очаговой пневмонией, фокальными кровотечениями, застоем крови. Пневмония часто (по данным Х. Эккерт, (1984) в 97%) сопровождается интерстициальным компонентом. Характерен интерстициальный отек, дисковидные ателектазы и плеврит. Пневмонии при системной красной волчанке обычно носят рецидивирующий характер, инфильтративные изменения в легких не исчезают под воздействием антибиотиков. По данным Е.М. Тареева с соавт. (1965), волчаночный пневмонит, как и другие болезни соединительной ткани, характеризуется гиалинозом альвеолярных мембран, очаговым некрозом стенки альвеол с капиллярными тромбами, участками организующейся интерстициальной пневмонии, кровоизлияниями и метаплазией бронхиолярного эпителия. На фоне волчаночного пневмонита и легочного васкулита наблюдаются различные осложнения: ателектаз, образование полостей буллезной эмфиземы, спонтанный пневмоторакс. Поражение интерстиция легкого сопровождающееся диффузным развитием соединительной ткани – пневмосклерозом, ограничением эластичности легочной ткани.
Легкие уменьшаются в объеме.
У 30–50% больных системной красной волчанкой имеет место выпот в плевральной полости.
Примерно в 4% случаев плеврит является первичным проявлением заболевания (E.L. Dubois,1966).
Дженнифер П. Mayberry, Стивен Л. Примак, Нестор Л. Мюллер
Морфологические изменения легких создают предпосылки к нарушению диффузии кислорода из-за развития альвеоло-капиллярного блока и к понижению парциального давления кислорода, что являются причиной часто наблюдаемого при волчаночном поражении легких нарушения дыхательной функции легкого. По этой же причине развивается гипертония в малом круге кровообращения с перегрузкой правого сердца.
Различают следующие клинические формы:
1) болезнь Леттерер–Зиве;
2) болезнь Хенда-Шюллера-Крисчена и 3) костная эозинофильная гранулема.
Эти болезни имеют различное течение, прогноз и клинические проявления. Этиология всех форм гистиоцитоза неизвестна.
Болезнь Леттерер-Зиве представляет острую форму диссеминированного гистиоцитоза Х с поражением костей, кожи и внутренних органов. Болезнь встречается только в раннем детском возрасте и обычно заканчивается летальным исходом в течение 1–2 лет.
Болезнь Хенд–Шюллер–Крисчена (липоидный гранулематоз) подострая форма гистиоцитоза Х. Она тоже встречается преимущественно в детском возрасте, но иногда поражает и взрослых.
Болезнь характеризуется триадой: поражением костей, экзофтальмом, и несахарным диабетом.
У взрослых, как правило, встречается первично-хроническая форма гистиоцитоза Х.
У взрослых гистиоцитоз Х, обычно проявляется в виде локальной формы – эозинофильного
гранулематоза. Болезнь более часто поражает мужчин в возрасте до 40 лет. Процесс локализуется преимущественно в костях. В 20% всех случаев изменения в скелете сочетаются с изменениями в легких. Поражение легких при этих двух формах гистиоцитоза встречается от 20 до 50% случаев (Л.И. Дмитриева и В.В. Ерохин, 1989; T.V. Colby и C. Lewbord, 1983). В 60% случаев наблюдается изолированное поражение легких. В 20% случаев изменения в легких сочетаются с поражением скелета.
Морфологически гистиоцитоз Х проявляется в виде множественных узелков гранулематозного характера размерами 2–3 мм. Другим характерным признаком легочного гистиоцитоза являются множественные кистоподобные полостные образования типа буллезной эмфиземы. Буллы, расположенные в периферических, субплевральных отделах могут лопаться, вследствие чего развивается спонтанный пневмоторакс. Гистологически гистиоцитоз Х характеризуется наличием крупных гистиоцитов (клеток Лангерганса), содержащих палочковидные и ракеткообразные органеллы. Гистиоцитарные гранулемы редко подвергаются некрозу, тем не менее, полостные образования в легких кистозного характера выявляются часто.
Клинические проявления легочных поражений не патогномоничны. Болезнь часто протекает бессимптомно. Нередко больные обращаются с неспецифическими респираторными жалобами. В далеко зашедшей стадии, когда фиброзный процесс захватывает обширные участки легких, развивается легочносердечная недостаточность.
Иногда больные обращаются к врачу по поводу различных жалоб со стороны скелета, типичными считаются жалобы на незаживающие луночки после удаления зуба. В большинстве случаев болезнь протекает доброкачественно. Часто наступает самопроизвольное излечение без какой-либо терапии.
В рентгенологическом изображении изменения легких при гистиоцитозе Х характеризуются двусторонним симметричным усилением легочного рисунка, вызванного диффузной гистиоцитарной пролиферацией в интерстициальной ткани и межальвеолярных перегородках, распространяющейся на альвеолы. Ведущим компонентом рентгенологической картины является склеротический процесс. На томограммах выявляется утолщение бронхиальных стенок с формированием перибронхиальных муфт. Инфильтрация и фиброз межальвеолярных перегородок вызывают формирование густой мелкоячеистой сети, на фоне которой видны буллезные вздутия. Все это придает легочному рисунку характер пчелиных сот. Изменения преобладают в средних, верхних и наружных участках легких (P.J. Friedman c соавт., 1981; J. Lacronique c соавт., 1982). В области пересечения тяжистых структур появляются утолщения, симулирующие мелкие узелки. Альвеолы местами полностью облитерированы, местами буллезно вздуты. Корни легких расширены за счет увеличения калибра магистральных ветвей легочной артерии на почве артериальной гипертензии (Л.И. Дмитриева и В.В. Ерохин,1989). Функциональные исследования в динамике позволяют обнаруживать затруднение капиллярного кровотока, преимущественно в верхних и наружных частях легких и нарастающую перегрузку правых полостей сердца.
Одним из наиболее характерных признаков гистиоцитоза Х является “сотовое легкое” – множественныe тонкостенныe мелкиe ячейки полости диаметром 3–4 мм и более, без выраженной перифокальной реакции на всем протяжении легочных полей (Е.М. Дембо, 1995; Ю.В. Малков, 1992; J. Collins, 2001; E.L. Kulwiec с соавт., 1992; U. Lorcher с соавт., 1991; A. Moore с соавт.,1989).
Сравнение разрешающих возможностей обычной рентгенографии и компьютерной томографии в выявлении “сотового легкого” показывает явное превосходство КТ. P.J. Friedman c соавт. (1981), J. Lacronique c соавт. (1982) показали, что на обычных рентгенограммах ячеистость сотового характера выявляется всего лишь в 1–15% гистицитоза Х. В то время как по данным M.W.Brauner (1989), A. Moore с соавт. (1989) при компьютерной томографии кисты являются доминирующим признаком гистиоцитоза легких в 70–90% случаев. Выявляемая на обзорных рентгенограммах ретикулярность легочного рисунка на компьютерных томограммах оказывается ячеистостью буллезного и сотового характера. На компьютерных томограммах высокого разрешения также часто выявляются мелкие узелки диаметром 5 мм.
D.P. Naidich c соавт. (1999) указывают на значительные трудности дифференцирования распадающихся гранулем и развивающихся на фоне пневмосклероза бронхоэктазов.
Облитерирующий бронхиолит.
Облитерирующий бронхиолит – это патологический процесс, развивающийся в глубоких дыхательных путях, характеризующийся пролиферацией фиброзной ткани в стенке или в просвете мелких бронхов и бронхиол. При патоморфологическом исследовании выявляют грануляционные бляшки в мелких дыхательных путях, которые распространяются на альвеолярные ходы и альвеолы. Процесс ведет к облитерации мелких дыхательных путей, к развитию пневмонита и очагового или диффузного пневмосклероза. Болезнь быстро прогрессирует и часто заканчивается смертью. Причина болезни не установлена. Облитерирующий бронхиолит может быть следствием неразрешившейся пневмонии, экзогенного аллергического альвеолита или одним из проявлений легочного поражения при коллагеновых болезнях, в частности, ревматоидном артрите, системной красной волчанке и пр. (A.G. Davison с соавт., 1983; G. FrancoisDevos с соавт.,2002; B.J. Mroz с соавт.,1997; H.H. Popper, 2002; D.R. Porter, 1992; J.H. Rees с соавт., 1991; Y.Shimizu с соавт., 2002; H. Tokuda, 2002).
Толчком к развитию ОБОП может быть ингаляция токсических веществ, особенно если они водорастворимы (R. Begin с соавт., 1982; T. Ezri с соавт.,1994; B. Godeau с соавт., 1991; S.J. Pegg c соавт., 1994; D.R. Porter, 1992; S.M. Weiss и S. Lakshminarayan, 1994). Описано сочетание облитерирующего бронхиолита с грануломатозом Вегенера, с синдромом Шегрена, с болезнью Стивенса–Джонсона. Многие авторы связывают развитие облитерирующего бронхиолита с инфекцией, например, вирусных инфекций, тропных к синцитиальному эпителию мелких дыхательных путей (респираторный синцитиальный вирус, цитомегаловирус, вирусы парагриппа, аденовирус, риновирус, корона-вирус и др.), к которым особенно восприимчив больной после трансплантации (G.B. Fischer с соавт., 2002; S. Husain и N. Singh, 2002; R. Trisolini с соавт., 2002).
Установлено развитие облитерирующего бронхиолита после приема некоторых лекарственных препаратов (R. Banka и M.J. Ward, 2002; P. Camus с соавт., 1993; K.J.Schwartzman с соавт.,1995), в результате радиационных повреждений после лучевой терапии (J.Kaufman и R.Komorowski, 1990; S.Kitagawa c соавт.,2003). Описаны случаи бронхиолита в сочетании с воспалительными заболеваниями толстой кишки (язвенным колитом и болезнью Крона) (P. Camus, с соавт., 1993; M.B. Casey c соавт., 2003; C.R. Swinburn c с соавт., 1988). В последнее время в связи с развитием трансплантологии появилось большое число публикаций с описанием облитерирующего бронхиолита у больных после пересадки комплекса сердце легкие, костного мозга и других органов (I. Khurshid и L. Anderson, 2002; S.M. Levine, 2002; J.P. Ouwens с соавт.,2002; I. Paradis c соавт., 1993; H. Paz с соавт., 1992; J.H. Rees c соавт. 1991. Предполагается, что данный синдром представляет собой проявление хронической реакции отторжения – реакции трансплантант против хозяина (В. Griffith и соавт., 1988; V.A. Holland с соавт.,1990; T.E. Jr. King, 1989). К. Bando с соавт., 1995; J.P. Scott с соавт. (1997) считают облитерирующий бронхиолит одним из основных препятствий на пути получения долгосрочных результатов пересадки легких. По их данным, облитерирующий бронхиолит развивается у 2/3 реципиентов. Использование более мощных иммунодепрессантов, таких как циклоспорин, азатиоприн, кортикостероиды, позволило значительно снизить частоту развития облитерирующего бронхиолита с 80% до 20–50% у больных после трансплантации легких (P. McCarty c соавт., 1990). Что касается пересадки костного мозга у больных с лейкозом или апластической анемией, то механизм развития облитерирующего бронхиолита у этих больных может быть связан не только с реакцией отторжения, но также с применением медикаментозных средств и сопутствующей инфекцией на фоне сниженного иммунитета. Еще одним фактором риска развития облитерирующего бронхиолита является хроническая ишемия трансплантированного легкого, связанная с поражением сосудов при реакции отторжения (К. Bando и соавт., 1995).
ОБ может развиться практически в любые сроки после трансплантации, хотя наиболее типичным является начало заболевания через 8–12 и более месяцев после операции (С.Н. Авдеев с соавт., 1998; О.Е. Авдеева с соавт., 1998; К. Bando с соавт., 1995; O. Brugiere с соавт., 2003; G. Devouassoux с соавт.,2002). O. Brugiere с соавт. (2003), T.M. Egan с соавт (2002), [93, 95] сообщили о повторных трансплантациях в связи с развитием облитерирующего бронхиолита в пересаженных легких. В тех случаях, когда не удается установить возникновение бронхиолита с какимилибо внешними или внутренними агентами, его называют идиопатическим или криптогенным. Учитывая столь большое многообразие различных по своей сути заболеваний, на фоне которых развивается облитерирующий бронхиолит, есть основания полагать, что ОБ является выражением неспецифической стереотипной реакции на различные повреждающие агенты.
Началом процесса может быть некроз бронхиолярной стенки, обнажение базальной мембраны, за которыми следует избыточная продукция различных регуляторных пептидов: факторов роста, цитокининов и адгезивных молекул (С.Н. Авдеев с соавт., 1998; P.M. Taylor с соавт..
Клинически болезнь напоминает грипп, проявляется лихорадкой, выраженной слабостью, кашлем, снижением жизненной емкости легких.
Рентгенологические проявления при облитерирующем бронхиолите многообразны. Наиболее часто выявляются множественные мелкие узелковые образования. Нередко наблюдаются участки понижения пневматизации инфильтративного типа. На компьютерных томограммах высокой разрешающей способности выявляются участки пониженной прозрачности слабой интенсивности в виде матового стекла при сохраненном сосудисто-бронхиальном рисунке или участков более интенсивного понижения пневматизации легочной ткани (консолидации) при исчезновении сосудисто-бронхиального рисунка. Интерстициальные изменения проявляются в виде сетчатости, вызванной утолщением междольковых перегородок и других линейных образований. Часто выявляются буллезные вздутия легочной паренхимы и трансформация легочной ткани по типу сотового легкого (П.В. Власов, 2004; J. Collins, 2001)
Экзогенный аллергический альвеолит
При иммунологическом исследовании обнаруживаются антигенспецифические (“иммунные”) розеткообразующие клетки.
Острая форма аллергического альвеолита сопровождается лихорадкой, ознобами, миалгиями, кашлем, одышкой, приступами удушья с признаками бронхоспазма. Ведущим симптомом хронической формы экзогенного аллергического альвеолита является прогрессирующая одышка рестриктивного характера, гипоксемия. Нарушение функции внешнего дыхания характеризуется снижением диффузионной способности легких и оксигенации артериальной крови.
Альвеолярный протеиноз.
В последнее время в литературе появилось большое число публикаций, посвященных малоизвестной, сравнительно редкой нозологической форме – так называемому альвеолярному протеинозу. Альвеолярный протеиноз – это своеобразное заболевание неизвестной этиологии, характеризующееся заполнением альвеол секретом липопротеинового состава. Болезнь встречается преимущественно у лиц среднего возраста (30–50 лет), причем у мужчин в 3–4 раза чаще.
Клинические проявления этого заболевания разнообразны. Наиболее частыми признаками является сухой кашель и одышка. Примерно у трети больных выслушиваются хрипы. При обследовании выявляется респираторная недостаточность, гипоксемия. Но примерно треть больных не предъявляют никаких жалоб (H. Asamoto, 1995; J.D. Godwin с соавт., 1988; S.E. Rossi с соавт., 2003).
Основным методом выявления альвеолярного протеиноза является рентгенологическое исследование, причем наибольшей информативностью обладает компьютерная томография высокго разрешения. Классическими признаками являются симметричная альвеолярная консолидация или слабо интенсивное понижение пневматизации типа “матового стекла”. При локализации в прикорневых зонах изменения напоминают отек легких. На компьютерных томограммах 85 до 100% выявляется двустороннее слабоинтенсивное однородное затемнение большей или меньшей протяженности в виде матового стекла, по форме напоминающее географическую карту, на фоне которого виден сосудистый рисунок. Вторым по частоте признаком является очаговое уплотнение легочной ткани. Его частота составляет около 80%. В этих случаях в легочной ткани определяются либо мелкие очаговые или более массивные фокусные тенеобразования. В некоторых случаях картина напоминает диссеминацию милиарного типа. Реже (примерно в 7% случаев) встречается выраженный междольковый и внутридольковый фиброз. Характерным для этого заболевания считается также симптом “булыжной мостовой” (crazypaving) (B. Coulier с соавт., 1999; C.E. Engeler c cоавт., 1993; S. Murayama c соавт., 1999; J.S. Park с соавт., (1995); S.E. Rossi с соавт., 2003).
Итак, в данной главе рассмотрениено несколько заболеваний легких (саркоидоз, идиопатический фиброзирующий альвеолит, гистиоцитоз, экзогенный аллергический альвеолит, альвеолярнгый протеиноз), объединенных в одну группу в силу определенного сходства рентгеноморфологическиих проявлений, основу которых составляет гранулематозные изменения, пневмосклероз и облитерация альвеолярного аппарата.. Общность морфологических изменений при заболеваниях данной группы можно объяснить стереотипом биологических реакций на различные этиологические факторы. Темпы развития каждой из рассмотренных болезней варьируют в широких пределах от острого до хронического. Однако в конечном счете больные погибают от легочно-сердечной недостаточности. Ведущим клиническим признаком всех рассмотренных в статье заболеваний является респираторная недостаточность. Имеется много общего в рентгенологических проявлениях всех рассмотренных болезней. Наиболее постоянными компонентами рентгенологической картины данной группы болезней является диффузный сетчато-линейный фиброз, диффузное слабо интенсивное понижение прозрачности типа матового стекла, буллезная эмфизема, трансформация легочной ткани типа “сотового легкого”.
Дифференциальная диагностика описанного круга заболеваний довольно трудна. Тем не менее, несмотря на определенное сходство морфологических изменений и рентгенологической картины при заболеваниях данного типа, точная нозологическая диагностика во многих случаях возможна при условии использования комплекса клинических, лабораторных и рентгенологических данных. Вместе с тем, несмотря на использование самых современных средств визуализации включая компьютерную томографию, точный нозологический диагноз во многих случаях возможен только при морфологическом исследовании.
Компьютерно- томографические признаки диффузных заболеваний легких
ГеоргиадиС.Г., Котляров П.М
Российский научный центр рентгено-радиолгии МЗ РФ
Лучевая диагностика и дифференциальная диагностика диффузных заболеваний легких (ДЗЛ) одна из сложных проблем рентгенологии. Диагностические ошибки в группе ДЗЛ составляют 50 - 75%, больные поздно подвергаются лечению - через 1,5-2 года после появления первых признаков заболевания. Ведущими в ранней диагностике ДЗЛ являются рентгенологические методы - рентгенография и рентгеновская компьютерная томография, ее методика высокого разрешения (КТВР). Имеются существенные трудности дифференциальной рентгенодиагностики различных нозологических групп ДЗЛ. Изменения вызывают идиопатические интерстициальные пневмонии (ИИП), бронхиолиты, гранулематозы (наиболее часто саркоидоз), диффузные поражения легочной ткани, обусловленные приемом лекарств, системными заболеваниями - ревматоидным артритом, красной волчанкой, склеродермией, рядом других заболеваний. Морфологические исследования выявляют различной степени воспалительную инфильтрацию интерстициальной ткани, альвеол, бронхиол. Изменения могут носить экссудативный характер или, наоборот, развиваются необратимые фиброзные изменения, редукция микроциркуляторного русла, разрушение альвеолярной ткани, констрикция бронхиол и, как следствие, нарушение газообмена, микроциркуляции( 1 -21).
Компьютерная томография с высоким разрешением увеличивает пространственную разрешающую способность в визуализации паренхимы легкого. Использование тонких срезов 1 - 2 мм и высоко-пространственный алгоритм реконструкции позволяет увеличить пространственную разрешающую способность. Практически все авторы единодушны, что РКТ является методом выбора в изучении тонкой макроструктуры легочной ткани, особенно изменений на уровне дольки, бронхиолы
Задача настоящей работы уточнение возможностей КТВР в визуализации дистальных отделов респираторного тракта и описание общей рентгенсемиотики изменения макроструктуры легких при диффузных заболеваниях.
Макроструктура дистальных отделов респираторного тракта в норме. Дистальные отделы респираторного тракта состоят из терминальных и респираторных бронхиол, ацинусов, долек легких. Мембранозные бронхиолы диаметром 1-3 мм, не имеют хрящевой ткани, толщиной стенки 0.3 мм, переходят в терминальные - около 0,7мм в диаметре, от которых отходят респираторные бронхиолы (0,6 мм в диаметре). Респираторные бронхиолы через поры связаны с альвеолами. Терминальные бронхиолы являются воздухопроводящими, респираторные принимают участие в проведении воздуха и газообмене. Общая площадь сечения терминального отдела респираторного тракта во много раз превышает площадь сечения трахеи и крупных бронхов (53-186 см. кв. против 7-14 см кв.), однако на долю бронхиол приходится только 20 % сопротивления воздухопотоку. В связи с малым сопротивлением терминальных отделов респираторного тракта, на ранних этапах поражение бронхиол может протекать бессимптомно, не сопровождаться изменениями функциональных тестов и являться случайной находкой при компьютерной томографии высокого разрешения (КТВР) легких. Дистальнее терминальной бронхиолы располагается ацинус, самая многочисленная структура легкого, в которой происходит газообмен, имеющий одну или несколько респираторных бронхиол. Величина ацинуса взрослых в диаметре 7 - 8 мм (схема 1).
Схема 1. Продольное сечение легочной дольки
При отсутствии патологических изменений КТВР не дифференцирует ацинус, хотя ацинарные артерии в ряде случаев могут визуализироваться.
Легочная долька (вторичная легочная долька)- наименьшая единица легкого ограниченная перегородками соединительной ткани. Вторичные легочные дольки состоят из 3 - 24 ацинусов. Центральная часть содержит легочную бронхиолу и артерию, которые при отсутствии патологичеких изменений, как правило, редко визуализируются при КТВР. Для их обозначения принят термин «центрилобулярная структура» (дольковое ядро). Центрилобулярные артерии имеют диаметр 1мм, ее ответвления - 0.5 - 0,7мм. Толщина стенки центрилобулярной терминальной бронхиолы около 0.15 мм. Вторичные легочные дольки разделены междольковыми перегородками, содержащими вены и лимфатические сосуды, артериальные и бронхиолярные ответвления в дольковом ядре. Вторичная легочная долька обычно полигональной формы с длиной каждой из составляющих сторон 1 - 2,5 см (схема 2).
Схема 2. Поперечное сечение легочной дольки
Соединительнотканный каркас дольки состоит из междольковых перегородок, внутридолькового, центрилобулярного, перибронховаскулярного, субплеврального интерстиция. Патологические изменения интерстициальной ткани дают разнообразную КТ изображении картину усиления легочного рисунка. Субплевральный интерстиций - представляет волокна соединительной ткани, связанные с висцеральной плеврой, покрывает поверхность легкого, распространяется по междолевым щелям. Наряду с междольковыми перегородками, субплевральный интерстиций представляет часть периферической системы соединительнотканного остова органа.
Междольковыеперегородки являются продолжением периферического интерстиция, распространяющегося по поверхности легкого ниже висцеральной плевры, содержат легочные вены и лимфатические протоки. Толщина неизмененной перегородки, которая в ряде случаев может визуализироваться при КТВР - около 0.1 мм. Внутридольковый интерстиций является частью периферического, сообщается с плевральной поверхностью.
Перибронховаскулярныйинтерстиций (бронховаскулярный пучок) представляет оболочку из соединительной ткани, охватывающую бронхи и сосуды от корней к периферии легкого. Центрилобулярный интерстиций является перибронхиолярным соединительно-тканным футляром. КТВР выявляет его при патологическом утолщении - в виде тонкой сети соединительной ткани в пределах альвеолярной ткани, вторичной дольки.
Симптом «матового стекла»Одним из общих признаков для ДЗЛ является наличие симптома «матового стекла», отображающего различные патологические изменения на уровне альвеол. Для доказательства наличия этого симптома необходимо выполнить КТВР. На сканах при обычной КТ (толщина среза 4 мм и более) из-за наложений данный симптом могут симулировать процессы в интерстиции, перибронховаскулярной зоне. В большинстве случаев симптом «матового стекла» указывает на активную, острую стадию развития ДЗЛ. Он соответствует альвеолиту, наличию в просвете альвеол клеточных инфильтратов (макрофагов, клеток крови, лимфоцитов и т.д.). Симптом проявляется снижением воздушности (прозрачности) альвеолярной ткани в виде низкой интенсивности «молочной пелены». В отличие от инфильтрации, фиброза легочной ткани на фоне «матового стекла» отчетливо прослеживается бронхо - васкулярные структуры легкого, зоны поражения четко отграничены от непораженной ткани. Изменения по распространенности могут быть диффузными, очаговыми смешанного характера. «Матовое стекло» отражает не только проявление альвеолита и воспалительной инфильтрации, аналогичный симптом возникает при застойных явлениях в микроциркуляторном русле или увеличении объема протекающей через капилляры крови (обозначается термином «мозаичная перфузия»).
«Мозаичная перфузия» («мозаичная гиповолемия») отличается от альвеолита природой возникновения «матового стекла». Пусковым механизмом является сосудистая обструкция дольковой артерии, гиповентиляции дольки или их сочетание. Возникает гиповолемия сосудистого русла дольки (обструктивного или спастического при гиповентиляции генеза), перераспределение крови, гиперволемия в неизмененой части легкого. При КТВР зоны «матового стекла» отображают ткань легкого с сохранной гемодинамикой(повышенная денсивность на КТВР). Зоны пониженной денсивности легочной ткани отображают нарушение микроциркуляции, гиповолемией. Для уточнения природы "матового стекла" проводится сравнительный анализ КТВР, сделанных на одном и том же уровне на вдохе и выдохе. При изменениях связанных с нарушением гемодинамики "матовое стекло" исчезает или уменьшает свою плотность по отношению к окружающим тканям на сканах выполненных на выдохе, в то время как симптом обусловленный альвеолитом имеет одну и туже плотность независимо от фаз дыхания.. Изменение макроструктуры легкого в виде сочетания «матового стекла» с уплотнением междольковых перегородок определяются как симптом «булыжной мостовой». Симптом отражает изменения как в альвеолах, так и уплотнение междольковых перегородок, внутридолькового интерстиция, отдельных очагов фиброза. Характерно четкое отграничение зон поражений от неизмененной ткани легкого. Наиболее характерен симптом «булыжной мостовой» для альваеолярного протеиноза, реже встречается при других ДЗЛ. Как и при «матовом стекле» на фоне изменений отчетливо пролеживаются бронхо-сосудистые структуры.
КТ семиотика патологических изменений интерстициальной ткани легкого при ДЗЛ.Уплотнение внутридолькового интерстиция приводит к появлению тонкого сетчатого или крупнопетлистого рисунка паренхимы легкого. Это ранний признак фиброза при многих диффузных заболеваниях легкого. Уплотнение перибронховаскулярного интерстиция, который окружает крупные бронхи и сосуды, проявляется уплотнением бронхиальной стенки, увеличением размеров или неравномерности просвета, четкообразности легочных артерий. Визуализация при КТВР терминальных, респираторных бронхиол в виде центрилобулярных очажков или "ветвистых структур", рядом с дилятированной артерией указывает на уплотнение внутридолькового интерстиция. Бронхиоло - артериолярные структуры могут иметь вид равномерного, четкообразного или очагового уплотнения, распологающегося в центре дольки, обозначается термином "уплотнение центрилобулярного интерстиция". Как правило обусловлен фиброзом соединительной ткани, окружающей бронхиолы и сосуды, реже лимфогенным распространением саркоидоза. Патологические изменения интерстиция можно классифицировать по морфологическому типу (фиброз, отек); варианту уплотнения (линейное, узловое, сетчато-узловое, их сочетание); локализации патологии относительно структур вторичной дольки. Для патологических изменений интерстиция характерно сетчатой формы усиление легочного рисунка за счет уплотнения междольковых, внутридольковых перегородок, внутридолькового интерстиция. Патологическое уплотнение междольковых перегородок, обычно результат фиброза, отека, или инфильтрации. Изменения можно подразделить на: 1)линейное уплотнение (затемнение) - любая удлиненная, тонкая мягкотканная линия в легочном поле. 2)паренхиматозный тяж - уплотнение в виде протяженной структуры. Термин используется для описания уплотнений толщиной несколько миллиметров, длиной 2 - 5 см и более, которые выявляются при легочном фиброзе, инфильтрации, отеке межуточной ткани. 3)прерывистое линейное уплотнение (1 - 3 мм толщиной) может быть внутридольковым или распространяться через несколько прилегающих легочных долек.У пациентов с лимфогенным распространением патологии (саркоидозе) наблюдается уплотнение междолькового и внутридолькового интерстиция. Уплотнения могут быть однородными, узловыми или смешанными (схема 3).
Схема 3. Варианты уплотнения интерстиция
Патологическое изменение - субплеврального интерстиция проявляется тонким, дугообразным уплотнением параллельно основному листку плевры, толщиной до нескольких миллиметров на расстоянии не более 1 см от плевральной поверхности. Субплевральные уплотнения обусловлены фиброзом, как правило, образуют единую сеть с уплотненными междольковыми перегородоками.
Мелкоочаговые образования. При ДЗЛ изменения затрагивают все структуры вторичной дольки, междольковый интерстиций. С помощью КТВР в ряде случаев можно точно говорить о принадлежности изменений к альвеолярным или интерстициальным структурам. Различают преимущественно хаотичную, перилимфатическую, центрилобулярную локализацию очажков, что в ряде случаев дает возможность предположить вероятную нозологию изменений.
Округлые, мелкоочаговые образования размером до 1 см хорошо выявляются при КТВР. Очажки подразделяются по размерам - на маленькие (до 1 см), большие (более 1 см), очажки 3-7 мм трактуются как микроузелок; по плотности - высокой и низкой денсивности; местоположению - центилобулярное, интерстициальное, перилимфатическое, субплевральное, хаотичное. Однако при анализе КТВР достоверно судить о локализации очажка в том или ином отделе паренхимы легкого не всегда возможно и нередко это предположительное заключение. В большинстве случаев при КТ выявляется хаотичное распределение очажков вокруг вторичной дольки и структур легкого. Характерна диффузно-очаговая локализация в легочной ткани - вдоль сосудов, плевральных поверхностях, междольковых перегородок с большими колебаниями на единицу площади. Хаотический характер распределения очажков наблюдается при гистиоцитозе, силикозе, милиарном туберкулезе, метастазах. Центрилобулярные очажки, узелки, соответствующие центру дольки, как правило, представляют фокус перебронхиолярного воспаления или инфильтрации легочной ткани (схема 4).
Cхема 4.Варианты очаговых изменений легких при ДЗЛ
Сочетание центилобулярных очажков с уплотненными, тонколинейными (1-2,5 мм) структурами указывает на их принадлежность к терминальным отделам респираторного тракта (симптом «ветки вербы с почками»). Субплеврально расположенные узелки визуализируются в виде цепочки по ходу основной или междолевой плевры. Характерны при саркоидозе и силикозе, носят наименование «псевдобляшек» (по аналогии с очаговым уплотнением париетальной плевру при асбестозе). Очажки, хаотично расположенные в легочной дольке могут отображать поражение дыхательных путей, внутридолькового интерстиция, разветвлений центрилобулярных артерий. Следует еще раз отметить трудности подразделения очажков на внутридольковые и воздушного пространства по данным КТВР.
Изменения мелких бронхов и бронхиол при ДЗЛ.Патологию бронхиального дерева можно разделить по локализации патологического процесса: изменения бронхов, бронхиол, структур дистальнее терминальных бронхиол. Наиболее частым следствием фиброза легких при ДЗЛ являются бронхоэктазы. Бронхоэктазы по виду делятся на цилиндрические, варикозные, кистозные. Первичная причина - дилятация стенок бронха в результате ее растягивания окружающей фиброзированной тканью(схема 5).
КТВР выявляет утолщение, неравномерность стенки, неровность просвета бронхов, жидкое содержимое (схема 5).
Схема 5. Варианты бронхиолоэктазов
Учитывая происхождение изменений в результате фиброза ткани изменения называются тракционными бронхо-, бронхиолоэктазами (в зависимости от уровня поражения). Одним из диагностических признаков бронхиолоэктазов является симптом «кольца с печаткой». При перпендикулярном положении по отношению к скану бронхососудистой структуры выявляется кольцевидная тень расширенного с утолщенной стенкой бронха, с прилежащим поперечным срезом легочной артерии (округлая мягкотканная структура). При дилятации, заполнении слизью, гноем, жидкостью, фиброзе просвета терминальной или респираторной бронхиолы по периферии легкого КТВР визуализирует линейно-ветвистые структуры с очажками (1-5мм) - симптом «ветки вербы». Симптом отображает патологию дистальных отделов респираторного тракта при бронхиолитах различного генеза, лимфоидной интерстициальной пневмонии, хронических инфекциях дыхательных путей. При проекции структур в плоскости КТ скана визуализируется ветвистая структура, напоминающая ветку весенней вербы с почками, перпендикулярно - изменения проявляются центрилобулярными очажками.
Кистозные изменения легочной ткани.Кисты легочной ткани - один из важных признаков ДЗЛ. Могут быть единственными, множественными, локализоваться в нижних, средних, верхних отделах легкого равномерно по всей паренхиме, субплеврально или в центральных зонах. Представляют полости с тонкой стенкой (< 3 мм), четко отграничены от окружающей ткани, диаметром 1 см и более, содержат, как правило, воздух, реже имеют жидкое содержимое (схема 6).
Схема 6 Кистозные изменения при ДЗЛ
Кисты имеют эпителиальную или соединительнотканную выстилку. Кисты при КТ выявляются при идиопатических интерстициальных пневмониях, саркоидозе, гистиоцитозе Х, ряде других ДЗЛ. Тракционные бронхоэктазы, которые нередки при фиброзе легких, могут приниматься за кисты, однако, кисты являются производными, расширенной альвеолярной ткани, окруженной стенкой различной толщены. Образование кист при ДЗЛ связано с легочным фиброзом, деструкцией легочной ткани, гибелью альвеол, потерей гроздьевидной структуры. Кистозные воздушные пространства группируются и разделяются фиброзной тканью, замещающей интерстиций. Конечной стадией фиброза легкого является замещение кист «сотовым легким» (кисты по типу «пчелиных сот»). Легочная ткань замещается кистозными воздушными пространствами диаметром от 3-10 мм до нескольких сантиметров (схема 6). «Сотовое легкое» (синоним "легкое «терминальной стадии») характерно для цирроза - где сочетаются кистозные полости, тракционные бронхоэктазы, поля фиброза с дезорганизацией макроструктуры легкого, редукцией микроциркуляторного русла, уменьшением диаметра магистральных сосудов по периферии легкого и расширением в области корней(легочная гипертензия).
Таким образом, КТВР выявляет целый ряд общих симптомов указывающих на ДЗЛ, стадию развития патологического процесса. Наиболее частые из них симптом "матового стекла", усиление легочного рисунка за счет уплотнения интерстициальной ткани, появление мелкоочажковых изменений в интерстиции, терминальных бронхиолах, нередко сопровождающихся нарушением вентиляции в альвеоляной ткани - возникновением воздушных ловушек. Другие симптомы - развитие кистозных изменений, тракционных бронхоэктазов возникают по мере прогрессирования заболевания, формирования необратимых фиброзных изменений.
Продолжение.
Аллергический альвеолит
Идиопатический легочной фиброз
Системная красная волчанка
http://www.learningradiology.com/lectures/chestlectures/Collagen%20Vascular%20Diseases-Lupus-2012/Collagen%20Vascular%20Diseases-Lupus-2012.html
Спасибо!
Спасибо на добром слове.