ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ КОСТЕЙ.
Опухоли костей составляют около 10% всех злокачественных новообразований у детей, которые встречаются преимущественно во втором десятилетии их жизни. В европейских странах, таких как Франция, Германия, Италия и Великобритания с населением 60-80 миллионов, ежегодно выявляются 200 случаев заболевания. Более чем 95% первичных опухолей костей у детей приходится на остеогенную саркому и саркому Юинга.
Остеогенная саркома
Остеосаркома - злокачественная опухоль, которая гистигенетически связана с примитивной мезенхимой или камбиальным ре зервом, обладающим потенцией к костеобразованию. В ней проис ходит прямое превращение опухолевой соединительной ткани в кость и остеоид. Ежегодно регистрируются 2-3 случая заболевания на один миллион населения. Остеогенная саркома может встречаться в лю бом возрасте, однако в 60% случаев приходится на второе десятиле тие жизни. Мальчики болеют ею чаще девочек (1,4:1) (рис. 52). При этом возраст заболевших девочек несколько ниже, чем мальчиков, что указывает на взаимосвязь между ускоренным ростом костей и развитием этих неоплазм (Link, Eilber, 1989). Более того, больные остеосаркомой обычно выше ростом по сравнению со своими свер стниками. Наиболее типичной локализацией опухоли являются метафизарные зоны быстрорастущих костей у подростков: нижний метафиз бедренной, верхний метафиз большеберцовой и плечевой кос тей. Реже опухоль поражает проксимальный отдел малоберцовой кос ти, позвонки, нижнюю челюсть.
В общем, можно отметить, что остеосаркома наиболее часто развивается в зонах наибольшего роста кости. На основе данных о 1043 больных, было отмечено, что опухоли располагались в следую щих областях скелета: у 269 (26%) - в большеберцовых костях, у 521 (50%) - в бедренных, у 102 (10%) - в плечевых костях, у 54 (5%) - в малоберцовой кости, у 40 (4%) - в костях таза, у 15 (1,4%) - в костях черепа, у 11 (1%) - в лучевой кости (рис. 53).
Рис. 53. Локализация остеогенной саркомы в костях скелета.
Представляется, что остеогенная саркома является злокачест венной трансформацией быстро пролиферирующих костноформирующих клеток, которая происходит вследствие случайного или индуцированного воздействия вирусных, химических или физиче ских агентов (Huvos, 1990).
Патоморфология
Микроскопически остеосаркоматозная ткань обычно компакт на, белесоватая и, вследствие наличия неопластических остеоидов, имеет твердую консистенцию. Степень опухолевого костеобразования бывает различной. Она может быть слабо выражена, и в таких остеолитических саркомах обычно обнаруживаются крупные кисты, очаги некроза, кровоизлияния, телеангиэктатические зоны (Ю. И. Соловьев, 1971).
В остеопластических саркомах, отличающихся интенсивным костеобразованием, на отдельных участках может происходить эбурнеация опухоли.
Микроскопически эта саркома отличается чрезвычайным струк турным полиморфизмом. Для опухолевой кости характерны атипизм клеток, костного вещества и архитектоники костных балок. Реак тивное костеобразование, так же как и лакунарная резорбция ста рой кости, представляет собой неспецифическую реакцию костной ткани. «Реактивная» кость то в виде редких тонких балочек, то в виде густой сети образуется по периферии опухоли, вблизи перио ста и представляет собой сформированную и равномерно обызвествляющую костную ткань (Соловьев Ю. Н., 1971).
Клеточные элементы варьируют от клеток, напоминающих по внешнему виду фибробласты и остеобласты, до многочисленных клеток ненормальной и причудливой формы.
Морфологический диагноз остеосаркомы должен основываться на совокупности разнообразия опухолевых структур и на наличии признаков опухолевого костеобразования.
Клиническая картина и диагностика заболевания
Как и при других первичных злокачественных опухолях кос тей, наиболее ранним симптомом является боль в области поражен ной кости, вначале проходящая, затем постоянная с увеличением ее интенсивности. По мере развития заболевания, в этой зоне выявля ется, становясь все более заметной, припухлость. В зависимости от подтипа опухоли, мягкотканный ее компонент может быть твердым или мягким. При быстром росте опухоли (что наблюдается у детей) может развиваться кахексия и прогрессирующая анемия. Возможны патологические переломы. Над опухолью иногда имеется сеть рас ширенных кровеносных сосудов. В некоторых случаях нарастает ак тивность щелочной фосфатазы, что отражает интенсивность про цессов костеобразования в опухоли.
Рентгенологическая картина остеогенной саркомы отличается большим разнообразием и во многом определяется морфологиче ским вариантом опухоли (остеопластическая, остеолитическая, сме шанная), локализацией и темпами роста. Наиболее характерные рентгенологические признаки проявляются при разрушении коркового слоя кости и при прорастании опухоли в мягкие ткани, т. е. уже в позднем периоде развития заболевания. При этом своеобразные из менения возникают в отслаивающемся периосте с образованием на границе дефекта коркового слоя и пораженных опухолью мягких тканей характерного «козырька» или «треугольной шпоры», распо ложенной под углом к длинной оси кости. Определенное диагно стическое значение имеет обнаружение так называемых «спикул» - реактивных костных разрастании, образующихся в мягких тканях при прорастании в них опухоли. «Спикулы» на рентгенограммах об разуют характерный радиакальный рисунок, располагаясь перпен дикулярно к длинной оси кости.
В зависимости от степени оссификации остеосарком, разли чают остеопластические, остеолитические или смешанные вариан ты опухоли. При оценке истинного интрамедуллярного и мягкотканного распространения опухоли простое рентгенологическое за ключение должно быть дополнено данными компьютерной томо графии (КТ) и, если возможно, магнитно-резонансной томогра фии (МРТ).
Радиоизотопное сканирование костей позволяет выявить нако пление радиоактивного препарата в области первичной опухоли и метастатических очагов других костей, которые встречаются при мерно в 5% случаев. Компьютерная и магнитно-резонансная томо графии могут помочь в диагностике распространенности опухоле вого процесса.
Артериография необходима при планировании органосохранного лечения. Однако с появлением МРТее роль значительно уменьшилась.
Около 10-20% больных имеют клинически выявляемые мета-стазы в период установления первичного диагноза заболевания. Лег кие - первая локализация их у 90% детей. Поэтому конвенциальная рентгенография грудной клетки в двух проекциях с дополни тельной компьютерной томографией являются обязательными ме тодами обследования при установлении стадии заболевания и по следующего планирования лечения. Около 10% детей с метастазами в легких, выявленными при установлении диагноза, имеют метастатические очаги опухоли в других костях. Для их выявления исполь зуется радиоизотопное исследование с радиоактивным технецием.
Многими исследователями отмечается, что имеется прямая за висимость между остеобластической активностью опухоли и уров нями сывороточной щелочной фосфатазы. Повышение ее содержа ния может быть показателем наличия остеосаркомы примерно у 50% больных (Rosen, 1975).
Выбор метода лечения в основном определяется морфологиче ским строением образования, поэтому обязательным компонентом диагностических исследований является биопсия. Чаще всего про водится трепанобиопсия с отпечатками с трепанобиоптата с после дующими гистологическими и цитологическими исследованиями. При сомнительном морфологическом заключении необходима от крытая биопсия для получения достоверного гистологического за ключения. Выполнение последней, по мнению Н. Н. Трапезникова (1968), несет меньшую опасность, чем тот реальный вред, который наносит неправильное лечение злокачественных опухолей.
Стадия
Определение стадии злокачественных опухолей костей в настоя щее время выполняется согласно классификации TNM (1987). Т - первичная опухоль.
ТХ - недостаточно данных для оценки первичной опухоли. Т0 - первичная опухоль не определяется. Т1 - опухоль ограничена надкостницей. Т2 - опухоль выходит за пределы надкостницы. N - регионарные лимфатические узлы. NX - недостаточно данных для определения состояния лим фоузлов.
N0 - метастазов в лимфоузлах нет. N1 - имеются метастазы в лимфоузлах. М - отдаленные метастазы.
MX - недостаточно данных для определения отдаленных ме тастазов.
М0 - отдаленных метастазов нет. Ml - имеются отдаленные метастазы.
PTNM - патогистологическая классификация. Категории рТ, pNи рМ соответствуют категориям Т, N, и М. G - степень дифференцировки опухолевых клеток. GX - степень дифференцирования не установлена. G1 - высокая степень дифференцировки. G2 - средняя степень дифференцировки. G3 - малодифференцированная опухоль. G4 - недифференцированная опухоль.
Примечание: саркома Юинга и первичная лимфома оцениваются как G4. Группировка по стадиям:
Стадия IA G1.2T1N0M0
Стадия I В G1.2T2N0M0
Стадия НА G3,4 T1N0M0
Стадия IIB G3,4 T2N0M0
Стадия III не устанавливается
СтадияIVA любое G, любое Т, N1,M0
Стадия IVB любое G, любое Т, любое N, Ml.
Метастазы
Большинство больных остеосаркомой, у которой выявляются отдаленные метастазы в процессе или сразу после окончания спе цифического лечения, имеют плохой прогноз. Однако большинст во этих метастазов реализуется в легких, что позволяет в ряде слу чаев произвести их полное хирургическое удаление. В последние 15 лет использование экономного хирургического лечения боль ных с метастазами остеосаркомы в легкие позволило значительно увеличить число длительно живущих больных (Beattie et al., 1975; Beron et al., 1988). Удаление легочных метастазов производится с минимальным удалением нормальной легочной ткани, т. е. чаще выполняется клиновидная их резекция (Martini et al., 1974). Если удается полностью резецировать все опухолевые отсевы, то 40- 50% больных живут длительные сроки наблюдения (Jurgens et al., 1988; Beron et al., 1988).
Необходимость использования при этом дополнительной хи миотерапии обсуждается. Однако ряд исследователей до оператив ного вмешательства рекомендуют проведение двух-трех курсов по лихимиотерапии и затем продолжать ее после операции у больных с III и IV-й степенями лекарственного патоморфоза в метастазах (Beron et al., 1988).
Факторы прогноза при первичной остеосаркоме
Для улучшения прогноза заболевания необходим строго инди видуальный подход к лечению каждого больного. Возможность его определяется, во многом, выбором тактики на основе знания основ ных факторов, влияющих на течение заболевания. Многочисленные исследования, проведенные в нашей стране и за рубежом и с ис пользованием одно- и многофакторного анализа, позволили выявить ряд таких прогностических факторов при остеосаркоме.
Так, например, Glasser et al. (1992), проведя однофакторный анализ данных о 279 больных с остеосаркомой II стадии выявили, что прогностическими факторами, значимо влияющими на продол жительность жизни, являются локализация первичной опухоли, ме-' стное излечение первичной опухоли и степень патоморфоза, разви вающегося после неоадъювантной системной химиотерапии. Даль нейший многофакторный анализ показал, что исход заболевания зависит только от локализации опухоли и степени патоморфоза. При этом было показано преобладающее значение в прогнозе последне го фактора. Число неудач лечения было почти в 5 раз выше в тех случаях, когда большая часть опухолевой ткани больных после хи миотерапии оставалась жизнеспособной по сравнению с имеющи ми полную регрессию опухоли.
У. У. Ишанходжаев (1993) на основании многофакторного анализа пришел к выводу, что наиболее существенными признаками, определяющими прогноз при остеогенной саркоме, являются раз меры первичной опухоли, рентгенологическая ее разновидность и терапевтический патоморфоз.
Саркома Юинга
Саркома Юинга - первичная высокозлокачественная опухоль некостного происхождения, обычно развивается в костях скелета, но иногда локализуется и в мягких тканях. Она составляет 10-15% всех первичных злокачественных новообразований костей. В год выявляется 0,6 новых случаев заболевания на 1 миллион населения (Prince, Jeffree, 1977). Эта саркома редко встречается у детей до 5 лет или у взрослых старше 30 лет. Пик заболеваемости наблюдается ме жду 10 и 15 годами жизни ребенка. Несколько чаще болеют мальчи ки (м:ж = 1,5:1) (рис. 54).
Патоморфология
Опухоль, развиваясь в костном мозге, диффузно инфильтриру ет его и затем, распространяясь на костную ткань, разрушает корко вый слой и поражает мягкие ткани. Макроскопически саркома Юинга представляет собой мягкую, рыхлую, серовато-белого цвета опухоль с зонами кровоизлияний и некрозов.
При гистологическом изучении она состоит из огромного ко личества тесно прилежащих друг к другу круглых клеток с неболь шими гиперхромными ядрами. Хроматин обычно распределен рав номерно, чаще пылевидный. Митозы встречаются редко. При гистохимическом исследовании в 90% случаев в протоплазме обнару живается гликоген.
Рутинное гистологическое описание сейчас дополняется иммуноцитохимическими и цитогенетическими исследованиями, позво ляющими лучше отдифференцировать саркому Юинга от других опухолей, состоящих из небольших круглых клеток. Нередко уста новлению диагноза препятствуют кровоизлияния, некрозы и другие дегенеративные изменения, а также воспалительные, лекарственные и реактивные явления, которые изменяют характерную для этих опухолей микроскопическую картину.
Клиническое течение и диагностика
Как и при других первичных злокачественных опухолях кос тей, преобладающими симптомами являются упорные боли и при пухлость в зоне поражения. Эти симптомы могут быстро нарастать за короткий период времени, или они могут не меняться в течение нескольких месяцев. Вовлечение периферических нервов приводит к развитию соответствующей неврологической симптоматики. Не редко у больных саркомой Юинга, особенно с быстротекущими формами этой болезни, клиническая картина имеет некоторые осо бенности, отличающие эту опухоль от других злокачественных но вообразований. У этих больных временами, наряду с общей разби тостью и нарастающей слабостью, определяется лихорадочное со стояние. Температура тела может достигать 39-40°С. Наряду с об щими явлениями, у многих детей кожа, покрывающая опухоль, уме ренно гиперемирована и горяча на ощупь. Наиболее часто опухо лью поражаются кости таза (20%), бедренная кость (19%), мало- и большеберцовые кости (11 и 10%), ребра (10%), позвоночник (8%) и плечевая кость (7%) (рис. 55). В отличие от остеосаркомы, при сар коме Юинга более часто поражаются плоские кости скелета. В длин ных трубчатых костях опухоль обычно исходит из диафиза или рас полагается в их центральных отделах, отличаясь этим от остеосарком, типично развивающихся в метафизах.
Рентгенологическая картина сарком Юинга весьма разнообраз на. Важное значение имеет выявляемая на рентгенограммах опухоль с локализацией в диафизарных отделах трубчатых костей. Далее рас познаванию саркомы Юинга может способствовать своеобразный характер деструктивных и продуктивных изменений в кости, возни кающих в процессе развития и роста опухоли. В рентгеновском изо бражении деструктивные и продуктивные изменения в кости выра жаются в разволокнении и разрыхлении коркового слоя и в проявлении нарастающих многослойных пластинчатых периостальных наслоений. В результате этих изменений пораженная опухолью кость приобретает характерное продольное слоистое строение, напоми нающее собой луковицу (С. А. Рейнберг, 1949). Вокруг патологиче ски измененной кости на снимках часто видна опухоль, инфильтри рующая мягкие ткани. Редко встречаются патологические переломы кости в месте развития опухоли (около 5% случаев). Саркомы ре берных костей иногда сопровождаются кровоизлияниями в плевру.
Картина конвенциальной рентгенографии обычно дополняется данными компьютерной или магнитно-резонансной томографии. Эти исследования помогают выявить границы интрамедуллярного рас пространения опухоли. Профильное радиоизотопное сканирование позволяет, кроме уточнения первичной опухоли, диагностировать метастатическое поражение других костей.
Наличие легочных метастазов определяется с помощью выпол нения рентгенограмм грудной клетки в двух проекциях и компьютер ной томографии. Аспирационная и/или трепанобиопсия костного моз га необходима для исключения поражения опухолью костного мозга.
Саркома Юинга - это быстро диссеминирующая опухоль. По литературным данным, число больных с клинически выявленными метастазами во время установления начального диагноза составляет 15-35% (Hayes et al., 1987). Из них около 50% находятся в легких и около 40% в других костях. Метастазы в лимфатических узлах встре чаются редко (менее 10%).
У детей может наблюдаться различной степени выраженности анемия и лейкоцитоз. Повышение сывороточной LDH связывается с неблагоприятным прогнозом.
Основными в диагностике сарком Юинга являются рентгено графическое, компьютерное (магнитно-резонансное) исследование пораженной кости, профильное радиоизотопное сканирование и мор фологическое изучение биоптатов, полученных после выполнения биопсии.
По распространенности заболевание подразделяется большин ством авторов на локализованное и диссеминированное. Хотя такое подразделение .сарком Юинга, в ряде случаев, носит условный ха рактер, что подтверждается тем, что несмотря на успешное излече ние местного очага поражения, у многих детей выявляются отдален ные метастазы в ближайшие сроки после лечения. Согласно класси фикации по системе TNM, саркома Юинга имеет только II (локали зованную) и IV стадии заболевания.
Метастазы
У больных саркомой Юинга во время установления диагноза в 10-35% случаев выявляются отдаленные метастазы. Прогноз заболе вания у этих детей значительно хуже, чем у больных с локализован ной формой болезни. При этом он несколько лучше у детей, имею щих легочные метастазы по сравнению с пациентами, у которых выявляются метастазы в кости. Лечение этих пациентов начинается с полихимиотерапии и дополняется проведением облучения. Для про ведения лечения рекомендуется использовать такие же схемы, что и при локализованной саркоме. Например, режим, предложенный Nesbit et al. (1990): 1. Первая фаза (0-8 недели) - винкристин 1,5 мг/м2, внутривенно, 1, 8, 15, 22, 29, 36 дни; циклофосфамид 500 мг/м2, внутривенно, 1, 8, 15, 22, 36 дни; доксорубицин 60 мг/м2, внутривенно, 36-й день; одновременно лучевая терапия первичной опухоли. 2. Вто рая фаза (9-68 недели) - дактиномицин 0,015 мг/кг, внутривенно, 1-5 дни; винкристин 1,5 мг/м2, внутривенно, 15, 22, 29, 36 дни; цик лофосфамид 500 мг/м2, внутривенно, 15, 22, 29, 36, 43 дни; доксору бицин 60 мг/м2, внутривенно, 43-й день. Лечение повторяется после перерывов длительностью 3 недели, 6 раз. 3. Фаза третья (69-98 неде ли) - дактиномицин 0,015 мг/кг, внутривенно, 1-5, 7 дни; винкри стин 1,5 мг/м2, внутривенно, 15, 22, 29, 36, 43 дни; циклофосфамид 500 мг/м2, внутривенно, 15, 22, 29, 36, 43 дни. Лечение повторяется 3 раза с перерывами в три недели.
В последующем периоде проводится тотальное или тотально-локальное облучение легких. В возрасте до 4-х лет доза излучения на всё легкое, по мнению Williams (1973), Carlos (1973), должна быть в пределах 12-15 Гр, подводимых по 1,5 Гр ежедневно 5 раз в неде лю (ВДФ =21). Pearson et al. (1964) проследили за судьбой 25 детей, получивших облучение легких в дозе 15 Гр. Только один больной умер через 18 лет от легочно-сердечной недостаточности, которая развивалась на фоне пневмофиброза.
У детей более старшего возраста радиотолерантность легоч ной ткани приближается к устойчивости взрослых людей, у кото рых облучение всего легкого в дозе 16 Гр (по 2 Гр 5 раз в неделю, ВДФ = 26) может привести к развитию плеврита только у 5% боль ных. При одновременном применении ионизирующих излучений и противоопухолевых лекарств такой же эффект может наблюдать ся, если суммарные дозы снижаются на 15-20%.
В НИИ ДО ОНЦ РАМН при лучевом лечении больных с легоч ными метастазами использовали методику гиперфракционирования. Поэтому мы сочли возможным тотальную дозу на легкое увеличить на 10-15%. При одностороннем поражении лучевому воздействию подверглось только одно легкое. На 1-м этапе оно облучалось в дозе 16,8 Гр (ВДФ = 26) с целью лечебного воздействия не только на клинически выявляемые метастазы, но и на субклинические их фор мы. Изоэффективная доза на метастазы при этом достигала 19 Гр (ВДФ =31). Суточная доза 2,4 Гр дробилась на два сеанса по 1,2 Гр за сеанс и с 4-часовым интервалом между последними; лечение про должалось 7 дней, давалось 14 фракций в неделю.
На 2-м этапе облучение продолжалось локально и только в зоне оставшихся метастазов по той же методике подведения форм излу чения.
При двустороннем поражении первично тотально облучалось наиболее пораженное метастазами легкое, затем второе. К локально му облучению метастазов в первом легком приступали через 2 недели по окончании тотального лучевого воздействия на второе. Оценива лась эффективность 1-го этапа лечения и, в случае наличия призна ков метастазов, проводилось локальное их дооблучение. И, наконец, аналогичная тактика была использована при определении необходи мости локального облучения отдаленных метастазов во втором лег ком. Величина доз и методика их подведения на каждое легкое и метастазы были аналогичны указанным выше.
Как показал анализ полученных данных, полная регрессия ме тастазов наблюдалась у 100% детей.
При множественных метастазах в кости, не пораженные ими зоны подлежат локальному облучению. При этом нет необходимо сти облучать всю кость, в которой локализуется метастаз (Wessal-owski et al., 1988). К сожалению, несмотря на хорошую начальную реакцию костных опухолевых очагов, только 10% детей живут 2 года без рецидива заболевания. Однако уже сейчас получены обнадежи вающие результаты при использовании интенсивных высокодозных курсов химиотерапии с пересадкой костного мозга (Burdachi, 1991). Но эти режимы находятся еще в стадии клинического изучения.






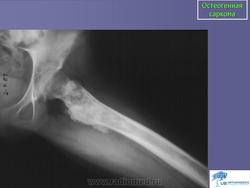


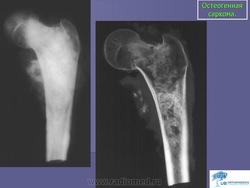

Саркома Юинга.
Остеоидная саркома. По частоте занимает первое место среди всех злокачественных новообразований костей, составляя, по данным разных авторов, от 30 до 80% первичных сарком скелета. Встречается преимущественно у лиц детского, юношеского и молодого возраста (10-30 лет). Несколько чаще болеют лица мужского пола. Поражает главным образом метафизы длинных трубчатых костей, составляющих коленный сустав (примерно половина наблюдений), а также плечевой кости. На первом месте стоит поражение бедренной, затем большеберцовой и плечевой костей. Реже опухоль локализуется в лопатке, костях таза, черепа и др. Главный симптом заболевания - боли, которые становятся постоянными, прогрессируют в своей интенсивности и оказываются мучительными. По мере развития процесса возникают и другие клинические признаки - припухлость, опухоль различной величины, расширение кожных вен, повышение местной температуры. Появляются хромота, иногда легкая контрактура в суставе. В некоторых случаях могут возникать патологические переломы. Для остеогенных сарком весьма характерно раннее метастазирование в легкие; метастазы в лимфатических узлах наблюдаются лишь в единичных случаях.
Рентгенологически различают три формы остеогенных сарком: остеолитическую, остеопластическую (склеротическую) и смешанную. Остеолитическая форма характеризуется появлением в кости очага деструкции различных размеров с нечеткими неровными контурами, который располагается обычно эксцентрически. На первых этапах заболевания периостальная реакция почти не выражена. В дальнейшем происходит разрушение коркового слоя, отчетливо выявляется периостальная реакция с образованием характерного периостального козырька. При остеопластической форме в очаге поражения кость неравномерно уплотнена, веретенообразно утолщена. По мере роста опухоли надкостница отслаивается и возникает периостальный козырек. Образуются игольчатые, пластинчатые, гребневидные или веерообразные периостальные разрастания (спикулы). Рост опухоли и разрушение костного вещества происходят в одинаковой степени как по длиннику, так и по поперечнику кости. Костно-мозговой канал довольно быстро выполняется опухолью, на фоне которой могут прослеживаться участки обызвествления.
В РОНЦ им. Н.Н. Блохина РАМН используют (в дополнение х TNM-классификации) следующие клинико-рентгенологические стадии, характеризующие течение остеогенной саркомы: I стадия - боль (периодическая, неопределенная), припухлость на уровне поражения, на рентгенограммах очаг поражения кости не распространяется за ее пределы; II стадия - боль (периодическая или постоянная), припухлость на уровне поражения, на рентгенограммах опухолевый очаг с поражением кортикального слоя, периостозы, внекостный компонент саркомы, метастазы в легком и скелете (отдаленные и skip-метастазы); III стадия - боль (постоянная, ночная), припухлость, нарушение функции конечности, на рентгенограммах обширные поражения кости, преимущественно всех ее слоев, распространение процесса на мягкие ткани, внекостный компонент, патологический перелом, отдаленные метастазы в легком и скелете.
В ряде случаев приходится проводить дифференциальную диагностику с доброкачественными образованиями, рентгенологически имитирующими остеогенную саркому. К ним относятся, в частности, доброкачественные костеобразующие опухоли, усталостные переломы, остеобластомы, другие менее злокачественные варианты остеогенной саркомы, как, например, паростальная остеосаркома. Порой трудно отличить иное высокодифференцированное образование, например фиброзную дисплазию, от фибробластической остеогенной саркомы low grade. При необходимости используют весь набор клинико-инструментальных и лабораторных методов исследования.
Диагноз остеогенной саркомы должен быть верифицирован гистологически с обязательным определением степени дифференцировки опухоли. Основными критериями для выработки лечебной тактики являются гистологический тип новообразования, биологические особенности, в частности степень злокачественности остеогенной саркомы в каждом конкретном случае, размер, объем, локализация, распространенность опухоли, общее состояние и возраст больного.
Наиболее неблагоприятный прогностический фактор при остеогенной саркоме - отдаленные метастазы: 5-летняя выживаемость больных с клинически выявленными метастазами составляет только 11%, а медиана выживаемости - 20 мес (P. Meyers et al., 1991).
Саркома Юинга. Занимает второе место по частоте после остеогенной саркомы, составляя от 10 до 16% всех злокачественных опухолей костей скелета. Заболевание встречается в основном у детей (10-15 лет, редко - моложе 5 лет), подростков и людей молодого возраста. Лица мужского пола поражаются примерно вдвое чаще, чем женского. Характерная локализация опухоли - метафизы и диафизы длинных трубчатых костей, кости таза, ребра, позвонки, хотя новообразование может встречаться в любом отделе скелета.
В начале заболевания появляются тупые боли в месте поражения, постоянно нарастающие и усиливающиеся по ночам. К числу ранних симптомов относятся повышение температуры тела вплоть до 39-400С, лейкоцитоз и увеличение СОЭ. По мере развития опухоли возникают внешние ее проявления в виде припухлости, покраснения кожи и других признаков воспалительного процесса. Боль может утихнуть, припухлость уменьшиться лейкоцитоз снизиться, но спустя некоторое время эти симптомы проявляются с новой силой. При пальпации опухоль имеет неравномерную консистенцию: участки хрящевой плотности чередуются с эластическими. Опухоль болезненна, неподвижна границы ее нечеткие, местная температура тела повышена. Адекватно интенсивности болевого синдрома и увеличению опухоли нарушается функция конечности. В некоторых случаях возникает патологический перелом. Рентгенологическая картина зависит от фазы развития заболевания. В начальном периоде в диафизе обнаруживаются мелкие, едва различимые очаги деструкции и некоторое отслоение надкостницы. Костномозговой канал расширен. В дальнейшем появляются крупные очаги просветления и типичная для саркомы Юинга периостальная реакция - слоистый, луковичного характера периостит, отдельные слои которого возникают с каждой новой вспышкой. Реже, в основном при быстром росте опухоли, наблюдается игольчатый лучистый периостит. Диафиз кости равномерно утолщается. При поражении плоских костей определяется обычно крупноочаговая деструкция без соответствующей периостальной реакции. Саркому Юинга следует дифференцировать в первую очередь с подострым остеомиелитом. Обязательна морфологическая верификация саркомы Юинга. Диагноз устанавливается на основании совокупности клинических, рентгенологических и микроскопических данных.
Характерные особенности саркомы Юинга - пестрота клинической картины, чрезвычайная агрессивность с бурным гематогенным метастазированием в кости (кости осевого скелета, череп, таз, позвоночник), легкие (45-65%), печень, а также в лимфатические узлы (20%) и др. По данным ряда авторов, срок появления метастазов в среднем составляет 11 мес.
Прогноз заболевания зависит от ряда факторов, в частности от исходной распространенности и локализации опухолевого процесса, гистологического варианта, характера лечения. По сводным данным на 1983 г., пятилетняя выживаемость больных саркомой Юинга варьировала от 4,5 до 24% (Н.Н. Трапезников с соавт., 1989). Успехи полихимиотерапии в современных программах комплексного лечения привели к существенному улучшению результатов: показатели пятилетней выживаемости достигают 60-70% (Н.Н. Трапезников с соавт., 1996, 1998).
Хондросаркома. Составляет 7-13% всех первичных злокачественных опухолей костей. Встречается обычно улиц старше 30 лет, поражая несколько чаще мужчин. В молодом возрасте хондросаркомы представлены в более злокачественном варианте. Локализуются преимущественно в длинных трубчатых костях, костях таза и грудной клетки. Различают центральную и периферическую формы хондросаркомы по отношению к самой кости. Вторичные хондросаркомы - малигнизация хрящевых новообразований - встречаются в 7-15 % случаев. Клиническое течение хондросарком относительно медленное, но вместе с тем встречаются и быстротекущие варианты заболевания, особенно у детей и подростков. Клиническая симптоматика хондросарком зависит от локализации опухоли в кости и вовлечения в процесс близлежащих органов и тканей. При периферических хондросаркомах ведущий симптом - появление медленно увеличивающейся неподвижной овальной плотной опухоли, которая может быть бугристой и болезненной при пальпации. В дальнейшем по мере роста опухоли присоединяются симптомы, связанные с давлением ее на нервные стволы и органы. Наиболее коварно протекают хондросаркомы отдельных участков тазовых костей, когда опухоль растет по направлению к тазовым органам. При центральных хондросаркомах ведущим симптомом являются боли, вначале незначительные и непостоянные, а затем усиливающиеся и беспокоящие больных даже в покое. Движения в близлежащем суставе ограничены и болезненны. После прорыва кортикального слоя опухоль выходит за пределы кости и инфильтрирует мягкие ткани. Метастазы хондросаркомы развиваются в относительно поздние сроки заболевания. Характерно гематогенное метастазирование (в легкие, печень, головной мозг), но возможно и лимфогенное - в регионарные лимфатические узлы. В распознавании хондросарком существенное значение принадлежит рентгенологическому методу. На рентгенограммах периферические хондросаркомы представлены плотной опухолью с нечеткими контурами, в центре которой отмечаются значительные обызвествления и множественные очаговые тяжистые обызвествления, идущие к периферии. Имеет место эрозия и умеренный склероз кости на поверхности, обращенной к прилежащей опухоли. При центральных хондросаркомах, локализующихся преимущественно в метафизах или метадиафизах, на рентгенограммах выявляется очаг деструкции овальной формы, распространяющийся на значительное протяжение по костномозговой полости. Кость веретенообразно вздута. Корковый слой утолщен, на некоторых участках может быть истончен или разрушен, что свидетельствует о выходе опухоли за пределы кости. На фоне опухоли выявляются характерные для хондросаркомы точечные или пятнистые обызвествления. Периостальные наслоения имеют слоистый или игольчатый рисунок, менее выраженный, чем при остеогенных саркомах. Хондросаркома может разрушить эпифизарный хрящ и прорасти в полость сустава. Клинико-рентгенологические данные, в том числе результаты компьютерной томографии, имеют существенное значение при диагностике хондросарком, однако диагноз должен быть верифицирован морфологическим исследованием с указанием степени дифференцировки опухолевых элементов. Следует вместе с тем иметь в виду, что взятый при биопсии кусочек новообразования может быть представлен доброкачественной или высокодифференцированной опухолевой тканью, тогда как рядом может располагаться более агрессивный участок опухоли, определяющий в конечном счете общую характеристику заболевания. Этот факт необходимо учитывать при формировании или коррекции окончательной лечебной программы.
Для большинства больных остается высоким риск местного рецидивирования. Что касается легочных метастазов, то они могут возникать достаточно поздно. При солитарных метастазах в легких, отсутствии метастазов в других органах, общем удовлетворительном состоянии больного может быть целесообразным хирургическое вмешательство на легком.
Прогноз. При высокодифференцированных хондросаркомах, доступных полному радикальному хирургическому лечению, 5- и 10-летняя выживаемость достаточно высока. Даже больные с опухолями таза, которые трудны для удаления, могут иметь средний срок выживаемости до 10 лет (при условии повторных хирургических вмешательств и проведения лучевой терапии). При низкодифференцированных формах хондросарком прогноз значительно хуже, и больные могут погибать в течение ближайших двух лет. В целом, поданным РОНЦ им. Н.Н. Блохина РАМН, 5-летняя выживаемость при первичной хондросаркоме составляет 39,8%, при вторичной - 81,4 % (Н.Н. Трапезников с соавт., 1983); такая разница объясняется тем, что при вторичной хондросаркоме обычно встречаются более дифференцированные варианты опухолей.
Выделяемые отдельно в современной гистологической классификации «дедифференцированные хондосаркомы» и «мезенхимальные хондросаркомы» отличаются более злокачественным течением и должны лечиться соответственно как «остеогенная саркома» и «саркома Юинга».
Злокачественная фиброзная гистиоцитома и фибросаркома кости. Эти злокачественные опухоли костей представляют собой сходные и практически идентичные нозологические единицы. Фибросаркома и злокачественная фиброзная гистиоцитома (ЗФГ) состоят из злокачественной веретеноклеточной стромы, в большинстве случаев обильно продуцирующей коллаген, а в младшей возрастной группе - остеоид. Встречаются редко (2-4% от всех первичных злокачественных опухолей костей), одинаково часто поражают лиц мужского и женского пола во всех возрастных группах. Существует точка зрения, что ЗФГ возникает в тканях с хроническим повреждением, отсюда и развитие опухолей с большой частотой в зонах облучения, областях инфаркта кости, в педжетоидных очагах и даже в виде дедифференцированной хондросаркомы.
В большинстве случаев рентгенологическая картина ЗФГ или фибросаркомы кости представлена литическим очагом. Локализация этих опухолей в костях скелета аналогична таковым при остеогенной саркоме, с преимущественным поражением бедренной, большеберцовой кости, костей таза, хотя опухоль может встречаться и в других костях скелета. Описываются как высокодифференцированные (low-grade), так и низкодифференцированные (high-grade) варианты ЗФГ и фибросаркомы. Они могут возникать как периостальные опухоли, подобно паростальной остеогенной саркоме, причем паростальная ЗФГ имеет низкую степень злокачественности. Фиброзная строма ЗФГ располагается циркулярно, а фибросаркомы - «линейно» или в виде «елочки», хотя чаще практически невозможно отличить одну опухоль от другой.
Клиническая картина ЗФГ и фибросаркомы имеет сходство с клиникой остеогенной саркомы: боль и наличие опухоли в пораженной области, которая при рентгенологическом исследовании имеет признаки злокачественного поражения кости. Литический характер опухоли часто приводит к развитию патологического перелома, наличие которого, как правило, является плохим прогностическим признаком, в частности при выполнении органосохраняющей операции, как и для выживаемости вообще.
Клиническое обследование при ЗФГ и фибросаркоме соответствует таковому при остеогенной саркоме.
Прогноз. По данным РОНЦ им. Н.Н. Блохина РАМН, в результате использования при лечении ЗФГ органосохраняющих операций с внутриартериальной предоперационной химиотерапией сначала адриамицином, а затем и цисплатином удалось снизить частоту рецидивов опухоли с 36,4 до 19,5% и повысить уровень 5-летней выживаемости на фоне адъювантной химиотерапии с 42,1 до 54,3% (Н.Н. Трапезников с соавт., 1998)
Саркома Юинга.
Хондросаркома.
Остеогенная саркома.
Саркома Юинга.
Продолжение.
Саркома Юинга.
Саркома Юинга.
Саркома Юинга
Саркома Юинга
Саркома Юинга
Опухоли костей
Radiology of Musculoskeletal Tumors | PDF Version
Остеосаркома
Osteosarcoma and its Variants | PDF Version
Остеоид остеома, остеобластома
Benign Osseous Tumors: Osteoid Osteoma, Osteoblastoma | PDF Version
Small Round Blue Cell Tumors: Eosinophilic Granuloma, Ewing's Sarcoma, Lymphoma, Myeloma | PDF Version
Опухоли костей.
Продолжение.
Продолжение.
Продолжение.
ВИДЕО.
Н.В. Кочергина - опухоли костно-мышечной системы: алгоритм лучевого исследования
https://www.youtube.com/watch?v=MeGvUODkaSQ
Н.В. Кочергина - Метастазы в костях
https://www.youtube.com/watch?v=53TpYnNDnbs