Муковисцидоз - заболевание с аутосомно-рецессивным типом наследования, обусловленное моногенной мутацией и характеризующееся поражением экзокринных желез в жизненно важных органах и системах.
Эпидемиология
Распространенность муковисцидоза варьирует в зависимости от популяции. В большинстве стран Европы и Северной Америки муковисцидозом заболевают от 1:2000 до 1:4000 новорожденных. По данным Медико-генетического научного центра РАМН, распространенность муковисцидоза в России составляет 1:12 000 новорожденных. Ежегодно в Москве рождается 10, в России - 300, в США - 2000, во Франции, Англии, Германии - от 500 до 800, а в мире - более 45 000 детей, больных муковисцидозом.
В России до сих пор большинство случаев заболевания не диагностируется или диагноз ставится в поздние сроки заболевания.
Классификация муковисцидоза
I. Формы муковисцидоза
• Смешанная (легочно-кишечная) с поражением желудочно-кишечного тракта и бронхолегочной системы (75-80%).
• Легочная (15-20%).
• Кишечная (5%).
II. Фаза и активность процесса
• Фаза ремиссии: • активность:
- малая;
- средняя.
• Фаза обострения.






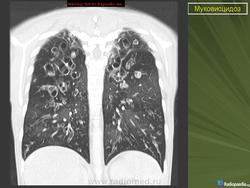




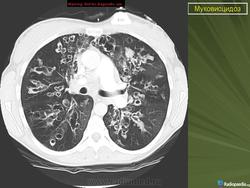

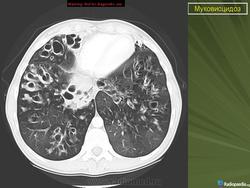




Этиология и патогенез заболевания
Муковисцидоз обусловлен мутацией гена МВТП (муковисцидозного трансмембранного регулятора проводимости), который расположен в середине длинного плеча 7-й хромосомы. На сегодняшний день выявлено более 1000 мутаций, ответственных за развитие симптомов муковисцидоза. Прогресс в изучении генетики муковисцидоза важен не только в перспективе генной терапии, но и возможности первичной его профилактики (предупреждение рождения ребенка, больного муковисцидозом).
В результате мутации гена секрет, вырабатываемый экзокринными железами, становится вязким, что обусловливает большинство процессов, лежащих в основе патогенеза заболевания.
Бронхолегочная система
Железы слизистой, выстилающей дыхательных путей, вырабатывают большое количество вязкого секрета, который скапливается в просвете бронхов и приводит к полной обтурации мелких бронхиол. В этих условиях у детей с муковисцидозом уже в течение первого года жизни или позднее, часто на фоне вирусной инфекции, снижающей эффективность локальных механизмов противомикробной защиты, в нижних дыхательных путях проникает большое количество различных патогенных и условно-патогенных микроорганизмов, чаще всего это:
• Staphylococcus aureus;
• Haemophilius influenzae;
• Pseudomonas aeruginosa.
В результате инфицирования неподвижной и вязкой слизи развивается гнойное воспаление. В условиях нарушения мукоцилиарного клиренса обструкция нарастает, что ведет к интенсификации инфекционного процесса и формированию порочного круга "обструкция - инфекция-воспаление".
Как правило, в первую очередь нижних дыхательных путей инфицируются S. aureus (наиболее часто выявляется в мокроте у пациентов с муковисцидозом первых лет жизни), затем часто присоединяется P. aeruginosa. Выявление P. aeruginosa, S. aureus и др. > 6 мес свидетельствует о хронической колонизации нижних дыхательных путей этими микроорганизмами. Прогрессирование хронического инфекционного процесса, вызванного P. Aeruginosa, обычно сопровождается нарастанием симптоматики, обусловленной поражением нижних дыхательных путей и прогрессивным ухудшением функции легких. При этом P. aeruginosa может трансформироваться в мукоидные (слизистые) формы, которые становятся нечувствительными к действию факторов иммунной защиты и противомикробных лекарственных средств. При хронической колонизации нижних дыхательных путей P. aeruginosa полная эрадикация возбудителя практически невозможна.
Бактериальная инфекция, обусловленная H. influenzae, часто развивается на фоне ОРВИ и может приводить у пациентов с муковисцидозом к выраженным дыхательным расстройствам.
В последнее время возросла роль Burkholderia cepacia. Течение инфекции, вызванной этим микроорганизмом при муковисцидозе, различно. Примерно у 1/3 больных отмечаются частые обострения бронхо-легочного процесса, развивается так называемый "cepaccia-синдром", характеризующийся молниеносной пневмонией и септицемией (прогноз при этом обычно плохой). У других больных она существенно не влияет на течение заболевания. Наличие в мокроте B. cepacia повышает риск развития суперинфекции, вызванной P. aeruginosa, S. aureus, H. influenzae.
Иногда в качестве случайной находки высевается другая патогенная микрофлора - Klebsiella pneumonie, Esche-richia coli, Serrata marcescens, Stenotrophomonas maltophilia и Proteus spp., однако роль этих микроорганизмов в патогенезе муковисцидоза окончательно не установлена.
Aspergillus fumigatus высевается из мокроты пациентов с муковисцидозом довольно часто. Наиболее клинически значимой формой грибковой инфекции при муковисцидозе является аллергический бронхолегочный аспергиллез, частота его развития у пациентов с муковисцидозом варьирует от 0,6 до 11%. При несвоевременной диагностике и в отсутствие адекватного лечения формируются проксимальные бронхоэктазы, отмечается быстрое прогрессирование бронхо-легочного процесса с нарастанием вентиляционных расстройств.
Современная концепция поражения легких при муковисцидозе указывает, что определенную роль в повреждении легочной ткани играют иммунные процессы. Иммунологические нарушения значительно возрастают при длительной колонизации нижних дыхательных путей P. aeruginosa. В процессе своего размножения микроколонии этого микроорганизма продуцируют вирулентные факторы, которые повреждают эпителий нижних дыхательных путей, стимулируют выработку медиаторов воспаления, повышают проницаемость капилляров, вызывают лейкоцитарную инфильтрацию.
Поджелудочная железа
Сгущение секрета поджелудочной железы часто приводит к обструкции ее протоков еще до рождения ребенка. В результате панкреатические ферменты, которые продолжают вырабатываться в ацинусах в обычном количестве, не достигают двенадцатиперстной кишки. Накопление активных ферментов приводит к аутолизу ткани поджелудочной железы. Часто уже на первом месяце жизни тело поджелудочной железы представляет собой скопление кист и фиброзной ткани (отсюда другое название заболевания - кистофиброз). В результате разрушения поджелудочной железы нарушаются процессы переваривания и всасывания (прежде всего жиров и белков), развивается дефицит жирорастворимых витаминов (А, Д, Е и К). При отсутствии соответствующего лечения это приводит к задержке физического развития ребенка. При некоторых мутациях гена муковисцидоза повреждение поджелудочной железы прогрессирует медленно, а ее функция остается сравнительно сохранной в течение многих лет.
Желудочно-кишечный тракт
Нарушения транспорта натрия, хлора и воды в тонкой кишке у новорожденных может приводить к закупорке дистальных ее отделов густым и вязким меконием - мекониальному илеусу. При этом в ряде случаев развивается атрезия тонкой кишки. Стенка чрезмерно расширенной кишки может разрываться еще до рождения ребенка, в результате развивается мекониальный перитонит.
У детей и взрослых также может возникать острая, подострая или хроническая обструкция дистальных отделов тонкой и проксимальных отделов толстой кишки клейким секретом слизистой и каловыми массами, приводящая к развитию кишечной непроходимости.
Другой причиной тонкокишечной непроходимости у детей с муковисцидозом может являться инвагинация тонкой кишки.
Задержка эвакуации содержимого из желудка, повышенная продукция соляной кислоты, нарушение перистальтики желудка часто приводят к развитию у пациентов с муковисцидозом гастроэозофагеального рефлюкса, развитию которого способствует также применение некоторых лекарственных средств, снижающих тонус нижнего пищеводного сфинктера (теофиллин, сальбутамол), или определенные виды физиотерапии. Из-за рецидивирующей или постоянной регургитации содержимого желудка в пищевод развивается эзофагит различной степени тяжести, иногда с развитием пищевода Барретта. При высоком желудочно-пищеводном рефлюксе возможна аспирация желудочного содержимого с аспирационным поражением легких.
Кожные покровы
Секрет потовых желез у пациентов с муковисцидозом характеризуется повышенными концентрациями натрия и хлора: содержание соли превышает нормальный показатель примерно в 5 раз. Такая аномалия функции потовых желез выявляется уже при рождении и сохраняется на протяжении всей жизни пациента. В условиях жаркого климата чрезмерная потеря соли через кожные покровы приводит к электролитным расстройствам, метаболическому алкалозу и предрасположенности к тепловому удару.
Репродуктивная система
Азооспермия у мужчин с муковисцидозом связана с врожденным отсутствием, атрофией или обструкцией семенного канатика. Указанные аномалии встречаются и у части лиц мужского пола из числа носителей гена муковисцидоза.
Снижение фертильности у женщин обусловлено повышением вязкости отделяемого цервикального канала матки, что затрудняет миграцию сперматозоидов.
Клинические признаки и симптомы болезни
Клинические проявления муковисцидоза зависят от поражения различных органов и систем и включают:
• признаки поражения бронхолегочной системы;
• признаки поражения поджелудочной железы;
• признаки поражения желудочно-кишечного тракта;
• признаки поражения гепатобиллиарной системы;
• нарушение потоотделения;
• нарушение репродуктивной функции.
Любой из указанных симптомов может наблюдаться у детей младшего или старшего возраста (известны нетипичные случаи появления симптома "барабанных палочек" и заболевания печени в первые годы жизни).
У большинства пациентов первые симптомы муковисцидоза выявляются уже на первом году жизни, хотя известны случаи более позднего, вплоть до зрелого возраста, развития заболевания. Симптоматика муковисцидоза в значительной степени зависит от типа мутации (или мутаций). Наиболее распространенной является мутация, при которой клинические признаки муковисцидоза появляются в раннем возрасте, развивается недостаточность поджелудочной железы (90% случаев).
Клинические проявления муковисцидоза в неонатальном периоде:
• мекониальный илеус (у 20% новорожденных с муковисцидозом), в ряде случаев перитонит, связанный с перфорацией кишечной стенки. До 70-80% детей с мекониальным илеусом больны муковисцидозом;
• длительная желтуха, которая выявляется у 50% пациентов с мекониальным илеусом.
Клинические проявления муковисцидоза на первом году жизни.
Для большинства детей грудного возраста, страдающих муковисцидозом, характерно сочетание следующих симптомов:
• кашель;
• нарушение стула;
• отставание в физическом развитии.
При этом один из них может выступать в качестве ведущего.
Кашель, сначала сухой и редкий, в дальнейшем прогрессирует до хронического, резкого, частого и мало продуктивного; приступы кашля могут провоцировать рвоту. В некоторых случаях он напоминает кашель больных коклюшем. Появление кашля может быть связано с инфекцией верхних дыхательных путей.
Для пациентов с муковисцидозом характерен частый, обильный, зловонный, маслянистый стул, содержащий непереваренные остатки пищи. Каловые массы с трудом смываются с горшка, пеленок, могут быть видимые примеси жира.
В некоторых случаях единственным симптомом заболевания может быть отставание в физическом развитии.
У 5% пациентов первым клиническим проявлением муковисцидоза может быть выпадение прямой кишки, к которому предрасполагают приступы кашля у детей с измененным стулом, недостаточностью питания, ослабленным мышечным тонусом, вздутием кишечника и эпизодическими запорами.
При тщательном обследовании обнаруживается учащенное дыхание, увеличение переднезаднего размера грудной клетки и слабо выраженное, но стойкое втяжение нижних межреберных мышц. Аускультативные патологические признаки могут вообще не выявляться или присутствовать в виде сухих и влажных мелко- и крупнопузырчатых хрипов. На рентгенограмме органов грудной полости выявляют уплотнение стенок бронхов, а также различной степени уплотнение или повышенную воздушность легочной ткани. Могут развиваться ателектазы в сегментах и долях легких, причем поражение правой верхней доли относится к диагностически значимым признакам муковисцидоза.
Манифестация муковисцидоза в дошкольном возрасте - достаточно редкое явление.
В отсутствие соответствующего лечения выпадение прямой кишки отмечается у 25% пациентов с муковисцидозом, как правило, в возрасте 1-2 лет. У детей старше 5 лет этот симптом встречается значительно реже.
Лишь в очень редких случаях диагноз муковисцидоза не устанавливается до достижения пациентами школьного возраста, что может быть связано с "мягкими" мутациями и относительной "сохранностью" функции поджелудочной железы.
Случаи манифестации муковисцидоза в подростковом и зрелом возрасте без каких-либо симптомов заболевания в анамнезе встречаются крайне редко и характеризуются менее типичными клиническими проявлениями.
Симптомы обострения бронхолегочного процесса у пациентов с муковисцидозом:
• изменение характера кашля;
• появление ночного кашля;
• увеличение количества мокроты и изменение ее характера;
• нарастание одышки;
• лихорадка;
• учащение пульса;
• ухудшение аппетита;
• снижение массы тела;
• снижение толерантности к физической нагрузке;
• цианоз;
• ухудшение физикальной и рентгенологической картины в легких;
• ухудшение показателей функции внешнего дыхания.
Осложнения муковисцидоза
Недостаток витамина Е проявляется гемолитической анемией у новорожденных и неврологической симптоматикой у детей старшего возраста.
Обструкция дистальных отделов тонкой кишки встречается у 2% детей младше 5 лет, у 27% пациентов в возрасте старше 30 лет, 7-15% пациентов всех возрастов.
Симптомы:
• боль в животе;
• пальпируемая увеличенная слепая кишка;
• частичная или полная кишечная обструкция крайне вязким содержимым илеоцекального отдела кишечника.
Тяжелая обструкция сопровождается болевым синдромом, вздутием кишечника, рвотой, запором и появлением уровней жидкости на обзорной рентгенограмме брюшной полости.
Такие осложнения, как назальный полипоз и холелитиаз, часто встречаются у пациентов с муковисцидозом и обычно протекают бессимптомно.
Клинические проявления аллергического бронхолегочного аспергиллеза.
По мере увеличения средней продолжительности жизни пациентов с муковисцидозом все чаще регистрируются такие поздние проявления и осложнения заболевания, как сахарный диабет и тяжелая печеночная патология, которые ранее из-за небольшой продолжительности жизни считались нетипичными для данного заболевания.
Сахарный диабет выявляется у 20% взрослых пациентов с муковисцидозом. Развитие сахарного диабета может быть спровоцировано терапией ГКС или высококалорийным питанием. Клинические проявления типичны для диабета - жажда, полиурия, полидипсия, снижение массы тела. Однако кетоацидоз при сахарном диабете, развившемся на фоне муковисцидоза, встречается редко.
Фиброз печени, развивающийся в той или иной степени почти у всех пациентов с муковисцидозом, в 5-10% наблюдений прогрессирует до тяжелого заболевания печени с билиарным циррозом и портальной гипертензией.
Диагноз и рекомендуемые клинические исследования
Диагноз муковисцидоза, как правило, ставят на основании типичных клинических проявлений заболевания в сочетании с высоким содержанием натрия и хлора в секрете потовых желез.
Отягощенный семейный анамнез
При диагностике муковисцидоза большое внимание уделяют выявлению отягощенного семейного анамнеза:
• наличие муковисцидоза у родных братьев или сестер;
• схожие клинические проявления у близких родственников или смерть детей на первом году жизни.
Потовая проба
Является наиболее специфичным диагностическим тестом муковисцидоза. Стандартная методика предусматривает сбор пота после ионофореза пилокарпина. У здоровых лиц концентрация натрия и хлоридов в секрете потовых желез не превышает 40 ммоль/л. Положительной потовой пробой считается концентрация хлора > 60 ммоль/л.
Показания к повторному проведению потовой пробы:
• положительная потовая проба;
• сомнительная потовая проба;
• результаты первой пробы отрицательные, но клинические проявления позволяют с высокой вероятностью предполагать наличие муковисцидоза.
Для окончательного диагностического заключения требуется получение положительных результатов при выполнении потовой пробы 2 или 3 раза.
Наиболее частые причины ложноотрицательных результатов:
• технические ошибки;
• проведение потовой пробы у новорожденных;
• безбелковые отеки или гипопротеинемия (по ликвидации отеков потовая проба становится положительной);
• лечение клоксациллином.
Ошибочные результаты обычно обусловлены различными техническими погрешностями - неаккуратностью при сборе и транспортировке пота, очистке кожных покровов, взвешивании и определении концентрации электролитов - и чаще всего возникают в лабораториях, редко проводящих анализ потовых проб.
Измерение разности назальных потенциалов
Измерение разности назальных потенциалов отражает основной дефект муковисцидоза и является информативным дополнительным методом его диагностики у детей старше 6-7 лет и взрослых. Суть метода состоит в измерении разности потенциалов между электродами, один из которых располагается на поверхности слизистой оболочки носа, а второй - на предплечье. В норме пределы разности потенциалов варьируют от -5 мВ до -40 мВ; у пациентов с муковисцидозом эти пределы составляют от -40 мВ до -90 мВ.
Генетический анализ
Генетическое тестирование на все возможные мутации, связанные с муковисцидозом, является слишком дорогим, так как число известных мутаций уже превышает 1000. Однако если ни одна из 10 наиболее часто встречающихся в данном регионе мутаций не обнаруживается ни в одной из хромосом пациента, вероятность диагноза муковисцидоза значительно снижается.
Неонатальная диагностика
Неонатальная диагностика позволяет:
• определить распространенность муковисцидоза в регионах, в которых диагностика муковисцидоза находится на недостаточно высоком уровне;
• своевременно выявить детей, страдающих с муковисцидозом, и как можно раньше начать соответствующее лечение;
• выявить семьи, нуждающиеся в генетической консультации.
Определение концентрации ИРТ в крови в настоящее время может использоваться как скрининговый метод для диагностики муковисцидоза у новорожденных. Концентрации ИРТ в крови новорожденных, страдающих с муковисцидозом, почти в 5-10 раз превосходят уровни ИРТ у здоровых детей. Однако необходимо отметить, что данный метод характеризуется низкой специфичностью. Если планируемая программа неонатальной диагностики включает определение уровня ИРТ, следует учитывать соотношение стоимости/эффективности подобных мероприятий.
Пренатальная диагностика муковисцидоза
Вероятность рождения ребенка с муковисцидозом в семье, где уже есть пациенты с этим заболеванием, составляет 25%. Современные возможности ДНК-диагностики позволяют выявить это заболевание уже во внутриутробном периоде и при необходимости прервать беременность.
Семьи, желающие иметь здорового ребенка, должны еще до планирования беременности провести ДНК-диагностику (ребенку с муковисцидозом, а также обоим родителям) и проконсультироваться у врача-генетика для получения заключения об информативности пренатальной диагностики муковисцидоза в данной семье. При возникновении каждой новой беременности семье необходимо сразу же (не позднее 8-й недели беременности) обратиться в центр дородовой диагностики, где на строго определенных сроках беременности врач-генетик проводит либо генетическую (8-12-я неделя беременности), либо биохимическую (18-20-я неделя беременности) диагностику муковисцидоза у плода. Отрицательные тесты позволяют гарантировать рождение здорового ребенка в 96-100% случаев.
Копрологическое исследование
У большинства пациентов с муковисцидозом обнаруживается недостаточность поджелудочной железы с очень низким уровнем или полным отсутствием панкреатических ферментов (липазы, амилазы и трипсина) в двенадцатиперстной кишке. При простом копрологическом исследовании выявляется выраженная стеаторея (в кале выявляются маслянистые капельки нейтрального жира). Это простое непрямое исследование функционального состояния поджелудочной железы в случае получения положительного результата значительно помогает в диагностике муковисцидоза.
Определение уровня эластазы-1 в кале (нормальное значение > 500 мкг/г) на сегодняшний день считается наиболее объективным методом выявления степени недостаточности экзокринной функции поджелудочной железы, не зависящим от проводимой заместительной терапии панкреатическими ферментами. Специфичность этого метода составляет 100%, чувствительность в выявлении панкреатической недостаточности у пациентов с муковисцидозом - 93%, а в постановке диагноза муковисцидоз - 86,6%.
Снижение количества эластазы-1 является показанием к назначению заместительной терапии ферментами поджелудочной железы и может помочь в подборе их доз.
Исследование функции внешнего дыхания
Является одним из основных критериев тяжести поражения органов дыхания у пациентов с муковисцидозом и оценки эффективности проводимой терапии. Диагностическая ценность исследования функции внешнего дыхания возрастает при обследовании детей старше 5-8 лет.
У детей с муковисцидозом возможно нарастание бронхиальной лабильности (гиперреактивности бронхов).
По мере прогрессирования хронического бронхолегочного процесса отмечается снижение объема форсированного выдоха за 1 секунду, жизненной емкости легких и форсированной жизненной емкости легких. Снижение указанных показателей на поздних стадиях заболевания связано с деструкцией паренхимы легких и нарастанием рестриктивных расстройств.
Исследование функции внешнего дыхания позволяет оценить уровень реакции бронхов на применение бронходилятаторов и выявить пациентов, у которых назначение данных лекарственных средств будет эффективным.
Генная терапия
Муковисцидоз стал одним из первых заболеваний, при котором начались разработки по генной терапии, продолжающиеся до настоящего времени. Комплиментарная ДНК уже клонирована.
Пациенты, страдающие с муковисцидозом, должны находится под диспансерным наблюдением регионарного центра муковисцидоза с обязательным обследованием 1 раз в 3 месяца, что позволяет следить за динамикой заболевания, своевременно выявлять осложнения и при необходимости корригировать терапию.
Перечень лабораторных и инструментальных исследований, которые должны быть проведены при амбулаторном осмотре пациента с муковисцидозом в поликлинике регионального центра муковисцидоза
• Исследования, которые необходимо проводить при каждом приеме пациента (1 раз в 3 мес)
- Антропометрия (рост, масса тела, дефицит массы тела).
- Общий анализ мочи.
- Копрологическое исследование.
- Клинический анализ крови (дополнительно при признаках обострения бронхолегочного процесса).
- Посев мокроты (при невозможности собрать мокроту - мазок с задней стенки глотки) на микрофлору и чувствительность к антибиотикам (дополнительно при признаках обострения бронхолегочного процесса).
- Исследование функции внешнего дыхания (дополнительно при признаках обострения брон-холегочного процесса).
- Определение SaO2 (дополнительно при признаках обострения бронхо-легочного процесса).
• Обязательное ежегодное обследование
- Биохимическое исследование крови (активность печеночных ферментов, электрофорез белков, электролиты, глюкоза).
- Рентгенография органов грудной клетки в прямой и правой боковой проекциях.
- Ультразвуковое исследование органов брюшной полости.
- Электрокардиография.
- Фиброэзофагогастродуоденоскопия.
- Осмотр отоларингологом.
- Тест на толерантность к глюкозе.
Диагностические критерии аллергического бронхолегочного аспергиллеза:
• нарастание симптомов поражения нижних дыхательных путей с появлением приступов бронхоспазма;
• новые рентгенологические изменения в легких (инфильтраты, ателектазы, сливающиеся, гомогенные затемнения или параллельные линейные тени);
• уровень общего IgE сыворотки крови > 500 МЕ/л или 4-кратное его повышение;
• повышение уровня специфичных IgE или положительный кожный тест с аллергеном А. fumigatus;
• повышенный уровень IgG к А. fumigatus;
• уровень эозинофилов крови > 0,5х109 /л и повышенное содержание эозинофилов в мокроте;
• выявление в мокроте А. fumigatus.
Для постановки диагноза необходимо наличие одновременно 4 и более из указанных критериев (наибольшее диагностическое значение из них имеют первые пять).
Дифференциальный диагноз
Хотя потовая проба и является специфическим методом диагностики муковисцидоза, существуют и другие заболевания, при которых она может быть положительной:
• синдром приобретенного иммунодефицита;
• недостаточность функции надпочечников;
• псевдогипоальдостеронизм;
• адреногенитальный синдром;
• синдром Дауна;
• синдром Клайнфельтера;
• атопический дерматит;
• эктодермальная дисплазия;
• семейный холестатический синдром;
• фукозидоз;
• гликогеноз II типа;
• недостаточность глюкозо-6-фосфатазы;
• гипотиреоз;
• гипопаратиреоз;
• кахексия;
• нервная анорексия;
• синдром Мориака;
• мукополисахаридоз;
• нефрогенный несахарный диабет;
• хронический панкреатит;
• гипогаммаглобулинемия;
• целиакия.
Продолжение.
Прошу прощения Валентин Львович! Небольшое дополнение к выше сказанному. Во Франции был певец Грегори Лемаршаль, очень талантливый молодой человек, в 12 лет чемпион Франции по акробатическому рок-н-роллу, выпустил 2 сольных альбома (исполнение просто супер!), умер в 23 года от муковисцидоза!!! После его смерти родители создали фонд Помощи детям больным муковисцидозом.
Спасибо за дополнение.