Металлоз — патологический процесс, развивающийся под влиянием металла, длительно находящегося в органе (глаз, кость); проявляется дистрофическими и пролиферативными изменениями.
Металлоз или металлические синовит.
Наблюдения Татьяны Валентиновны.
Немного комментариев к снимкам:
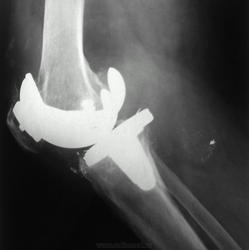
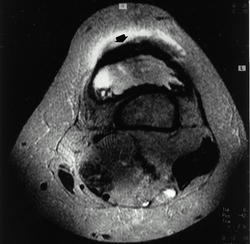
Все снимки сделаны через 10-30 лет после эндопротезирования
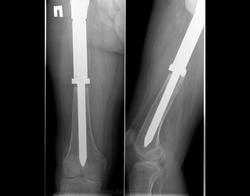
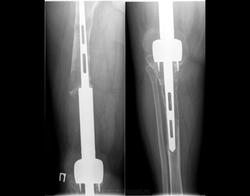
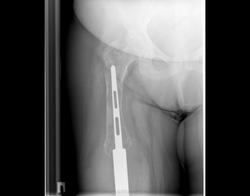
Снимки 4,5,6 пациентки, которой была сделана резекция бедренной кости с эндопротезированием коленного сустава 30 лет назад по поводу остеосаркомы. Расшатывание эндопротеза клинически стало себя проявлять 5 лет назад (снимок 4), далее довольно быстро прогрессировало, что по-видимому усугубилось присоединившимся остеомиелитом (снимки 5, 6 - теперешние). Пришлось выполнить ампутацию, тем не менее, человеку дали 25 лет нормальной, полноценной жизни.




Онкологический Научный Центр имени Н. Н. Блохина РАМН,
Центральный институт травматологии и ортопедии имени Н. Н. Приорова.
С. А. Ягников, В. Н. Митин, Н. С. Гаврюшенко
В эпоху эндопротезирования возник ранее неизвестный термин металлоз, означающий интенсивное засорение мягких тканей продуктами износа эндопротеза. Металлоз и нестабильность эндопротеза стали синонимами, а асептическое воспаление и металлоз — неразлучными спутниками.
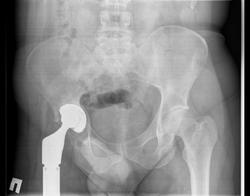
Остеолиз, возникающий на периферийной части эндопротеза в позднем послеоперационном периоде, является основным осложнением тотального замещения тазобедренного сустава у человека и собаки (фото 1).
Это связано с тем, что продукты износа металла и полиэтилена, образующиеся в узле трения эндопротезов, распределяются по всей контактной поверхности кость-имплантат. Последующая реакция остеобластов на частицы износа приводит к выработке большого количества простагландинов Е2, индуцирующих активизацию остеокластов, которые в свою очередь вызывают резорбцию кости (1; 5; 6; 7; 10; 11; 12). Продукты износа — это основной промотер асептической нестабильности как бедренного, так и вертлужного компонентов эндопротеза (1; 3; 4; 5; 6; 7; 8; 9; 10; 11; 12; 13). Возрастающее давление юридических аспектов на ветеринарную практику, а также увеличивающееся число молодых животных, нуждающихся в тотальном замещении тазобедренного сустава эндопротезом, диктуют необходимость удлинения времени износа имплантата, что позволяет избежать ревизионных операций. Эксплуатационные свойства узла трения эндопротеза зависят от структуры его металла, шероховатости трущихся поверхностей и коэффициента трения. Все эти параметры могут быть выверены в условиях лаборатории. Полученные результаты позволяют прогнозировать долговечность имплантата после тотального замещения тазобедренного сустава (2; 3; 4; 6; 9).
ЦЕЛЬ И ЗАДАЧИ ИССЛЕДОВАНИЯ
Цель работы — сравнить трибологические* свойства пар трения эндопротезов тазобедренных суставов для собак, имеющихся на отечественном рынке.
Для осуществления поставленной цели необходимо:
1) Оценить шероховатость поверхностей головок и вертлужных компонентов эндопротезов.
2) Определить коэффициент трения в узле трения эндопротезов.
3) Определить линейный износ в парах трения эндопротезов.
4) Изучить структуру металла эндопротезов, механические свойства и химический состав.
МАТЕРИАЛЫ И МЕТОДЫ
Исследованию были подвергнуты 5 неразъемных эндопротезов с металл — металлической парой трения (CoCrMo/СоСгМо) по типу К.М. Сиваша Государственного экспериментального предприятия Центрального института травматологии и ортопедии им. Н.Н. Приорова (ГЭП «ЦИТО») и пять разъемных эндопротезов с металлополимерной парой трения (головка — СоСгМо/вертлужный компонент — высокомолекулярный полиэтилен) Швейцарской фирмы MATHYS (фото 2).
Определение шероховатости поверхности головок и вертлужных компонентов эндопротезов определяли на поворотном талисерфе фирмы «Тейлор-Хобсон» №112/818. Алмазная игла прибора сканировала поверхность головок и вертлужных компонентов эндопротезов и записывала информацию на бумагу с увеличением 20.000х и 50.000х (рис. 1а и 1б). По диаграмме определяли параметры шероховатости головок и вертлужных компонентов эндопротезов:
1. среднее арифметическое отклонение профиля (Ra)
2. высоту неровностей профиля по десяти точкам (Rz)
3. базовую длину шероховатости (L)
На основании параметров шероховатости поверхностей головок и вертлужных компонентов эндопротезов по таблице 1 определяли класс обработки узла трения эндопротезов.
Определение коэффициента трения проводили на универсальной испытательной машине Zwick 1464 (фото 3). При испытании использовали два датчика: датчик силы (шкала 1 кН — 1000 Н) и датчик крутящих моментов (шкала 5 Нм). Образцы закрепляли в трехкулачковые зажимы. Осевая нагрузка в узле трения составила 300 Н, что соответствует величине средней вертикальной составляющей реакции опоры тазовой конечности собаки весом 40-45 кг. Для приближения условий испытаний к реальным в пары трения эндопротезов добавляли синовиальную жидкость из суставов здоровых доноров. Скорость вращения в эксперименте — 1 Гц (один оборот в секунду).
Программировали от 50 до 150 оборотов в испытательной машине, что соответствует сроку службы эндопротеза при замещении тазобедренного сустава = от 3 до 6 лет [4].Для расчета коэффициента трения использовали формулу Н.С. Гаврюшенко.
Ктр.=Мкр./P x r, где
Ктр. — коэффициент трения
Мкр. — крутящий момент (Нм), определяется экспериментально в лаборатории на машине Zwick.
Р — нагрузка на узел трения,
R — радиус головки эндопротеза (м).
Линейный износ узлов трения эндопротезов определяли на машине фирмы «Тейлор-Хобсон», сравнивая размеры головок и вертлужных компонентов эндопротезов до и после испытания на машине Zwick. Микроскопически исследовали синовиальную жидкость на наличие продуктов износа после завершения циклических испытаний.
Металлографическое исследование головок, вертлужных компонентов и ножек эндопротезов проводили по стандартной методике. Образцы подвергали тонкой шлифовке наждачной бумагой различных номеров и окончательной электрополировке в растворе следующего состава: 20% хлорной кислоты (НСЮ4, плотность 1,6 г/см3), 80% уксусной кислоты (СНЗСООН, плотность 1 г/см3). Использовали катод из аустенитной** нержавеющей стали, напряжение на электроде 50 — 60 В. Электрополировку проводили в стеклянном водоохлажденном сосуде. Химическое травление для выявления структуры проводили в растворе: 40 мл Н2О+480 мл HCI+48 г CuCI2. Для исследования микроструктуры использовали оптический микроскоп Neofot-21 (Karl Zeiss, Германия), максимальное увеличение 1000″.
Механические свойства узлов трения эндопротезов (предел текучести, предел прочности, относительное удлинение на разрыв) определяли на универсальной испытательной машине Zwick.
Химический состав металлов отечественных и импортных эндопротезов получен из конструкторских подразделений предприятий — изготовителей.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Параметры шероховатости головок и вертлужных компонентов эндопротезов ГЭП «ЦИТО» имели следующие средние значения:
1. среднее арифметическое отклонение профиля (Ra) — 0,32 мкм
2. высота неровностей профиля по десяти точкам (Rz) -1,47 мкм
3. базовая длина шероховатости (L) — 0,25 мм, что соответствует 9 классу обработки трущихся поверхностей имплантатов.
Эндопротезы фирмы MATHYS имели 12 класс обработки имплантата. Параметры шероховатости головок и вертлужных компонентов имели следующие средние значения:
1. среднее арифметическое отклонение профиля (Ra) — 0,020 мкм
2. высота неровностей профиля по десяти точкам (Rz) — 0,100 мкм
3. базовая длина шероховатости (L) — 0,09 мм
Значения крутящего момента эндопротезов ГЭП «ЦИТО» находились в пределах 1,2- 1,4 (среднее значение — 1,33) Нм, в протезах фирмы MATHYS 0,7 — 0,8 (0,78) Нм. При введении в узлы трения эндопротезов синовиальной жидкости крутящий момент снизился в среднем до 0,59 (0,52 — 0,65) и 0,56 (0,52- 0,62), соответственно (табл. 2).
Коэффициент трения, рассчитанный по формуле Н.С. Гаврюшенко, в протезах ГЭП ЦИТО при сухом трении имел значения от 0,8 до 0,93 (0,89), а при введении в узел трения синовиальной жидкости от 0,35 до 0,43 (0,39). В эндопротезах фирмы MATHYS 0,32 (от 0,29 до 0,37) при сухом трении и 0,23 (0,22-0,26) при добавлении синовиальной жидкости (табл. 2).
Ежегодный линейный износ в метало — полимерной паре трения эндопротезов фирмы MATHYS составил 0,1 — 0,2 мм/год за счет износа высокомолекулярного полиэтилена. Цвет синовиальной жидкости не изменился после циклических испытаний. Микроскопически в ней не обнаружены продукты износа.
В паре трения металл — металлических эндопротезов ГЭП «ЦИТО» линейный износ составил 0,4 — 0,7 мм/год (разрушение головки и вертлужного компонентов). Отмечено, что в металл — металлической паре трения ежегодный линейный износ снижался при увеличении срока службы эндопротезов. Синовиальная жидкость после циклических испытаний имела насыщенно-черный цвет (фото 4). Микроскопически в синовиальной жидкости выявлены продукты износа узла трения имплантата.
Металлографические исследования эндопротезов ГЭП «ЦИТО» показали, что поверхностный слой головок и вкладыши вертлужных компонентов изготовлены из литого сплава CoCrMo (ISO 5832/4), имеют неравновесную дендритную структуру. В структуре четко выявляется эвтектический*** карбид (преимущественно хрома) размером до 12-20 мкм (фото 5). Основа вертлужного компонента эндопротеза, шейка и ножка изготовлены из титанового сплава ВТ 6 (фото 6).
Бедренные компоненты эндопротезов фирмы MATHYS (головка, шейка, ножка) изготовлены из деформируемого кованного сплава CoCrMo (ISO 5832/6), который имеет однофазную структуру, представленную равноостными зернами альфа-кобальта, имеющего гранецентрическую гексагональную решетку. В структуре металла выявляются равномерно распределенные мельчайшие зерна карбида М23С6 и М7СЗ. Их размеры составляют 2 — 3 мкм (фото 7). Вертлужный компонент изготовлен из высокомолекулярного полиэтилена.
Механические свойства кобальтовых сплавов, используемых для изготовления эндопротезов, представлены в таблице 3.
Химический состав комохромовых сплавов, используемых для производства эндопротезов, представлен в таблице 4.
ОБСУЖДЕНИЕ
Металлографические исследования показали, что структура металла, используемого для изготовления швейцарских эндопротезов, достигается вакуумной плавкой с последующей «ковкой» металла — прессацией. Однородная мелкозернистая структура металла представлена СоСгМо матрицей с равномерно инкорпорированными карбидами высокой прочности. Такое распределение мельчайших карбидов (2-3 мкм), достигаемое данной технологией, и структура металла позволяют снизить шероховатость при обработке трущихся поверхностей узла трения. Мельчайшие карбиды не выкрашиваются при обработке трущихся поверхностей и создают единую, ровную, прочную поверхность с матрицей, состоящей из СоСrМо.
Эндопротезы ГЭП ЦИТО изготовлены из литьевого комохрома. Неравномерное распределение карбидов-»гигантов» (12 -20 мкм) в матрице приводит к их «выкрашиванию» при шлифовке поверхностей. Выпавшие из матрикса карбиды оставляют лунки. Дальнейшая шлифовка приводит к сглаживанию лунок, но на поверхности появляются другие карбиды, которые повторяют неровность трущейся поверхности. Прочность карбида в несколько раз превосходит прочность матрицы.
Наличие карбидов-»гигантов» не позволяет выполнить шлифовку поверхности с низкими параметрами шероховатости, что определяет невысокий класс обработки узла трения эндопротезов ГЭП «ЦИТО». Значения момента кручения и коэффициента трения показали зависимость этих параметров от класса шлифовки поверхностей узлов трения эндопротезов.
Эндопротезы тазобедренного сустава ГЭП «ЦИТО» в условиях сухого трения имели высокую степень сопротивления движению, что подтверждается высоким крутящим моментом (1,33 Нм) и коэффициентом трения (0,89). При добавлении в узел трения синовиальной жидкости указанные величины снизились на 44,4% и 43,8% соответственно.
Металло-полимерные эндопротезы фирмы MATHYS в условиях сухого и влажного трения имели меньшую по сравнению с металлическими эндопротезами ГЭП «ЦИТО» степень сопротивления движению. В условиях сухого трения крутящий момент был на 70,5 % ниже, чем в эндопротезах отечественного производства, а коэффициент трения на 178 %. При добавлении в узел трения синовиальной жидкости разница между имплантатами составила 5 и 69,6% соответственно.
Резкое снижение момента кручения и, как следствие, коэффициента трения в эндопротезах ГЭП «ЦИТО» при добавлении в узел трения синовиальной жидкости, вызвано её смазывающими свойствами, достаточным проникновением и равномерным распространением синовиальной жидкости между трущимися поверхностями узла трения. Отсутствие данного эффекта у импортных эндопротезов, на наш взгляд, является следствием минимального зазора между трущимися поверхностями головки и вертлужного компонентов эндопротеза. Трущиеся поверхности по этой причине не полностью разделяются смазкой и находятся в контакте.
Линейный износ трущихся поверхностей эндопротеза зависит от параметров шероховатости и коэффициента трения. Повышенный износ в паре трения металл-металлического эндопротеза ГЭП «ЦИТО» обусловлен низким классом шлифовки трущихся поверхностей и высоким коэффициентом трения (фото 8). Карбиды-»гиганты» в узле трения эндопротеза как алмаз стеклореза, ведомый по стеклу, приводят к разрушению матрицы головки и вертлужного компонента эндопротеза. Частицы износа (карбиды, металл) в узле трения эндопротеза продолжают разрушающее действие. Малый диаметр головки эндопротеза (10мм) обуславливает более высокое давление на единицу поверхности вертлужного компонента, что также способствует увеличению коэффициента трения и линейному износу.
Постепенное снижение износа в паре трения металл-металлического эндопротеза, по-видимому, происходит за счет прослойки, напоминающей «смазку шрус», которая образуется при смешивании частиц металла и синовиальной жидкости. Микроскопическое исследование изменившей цвет синовиальной жидкости показало наличие в ней продуктов износа. Морфологические исследования in vivo подтвердили наличие продуктов износа в полости капсулы сустава и периартикулярных тканях.
В эндопротезах фирмы MATHYS линейный износ отмечен в вертлужном компоненте эндопротеза, изготовленном из сверхвысокомолекулярного полиэтилена.
Виновником износа является стеарат кальция, который выкрашивается из полиэтилена, оставляя мельчайшие воронки. При микроскопическом исследовании синовиальной жидкости продукты износа в ней не выявлены. Однако морфологические исследования детрита из полости капсулы эндопротеза in vivo выявили наличие металлических частиц.
Частицы износа эндопротезов не остаются в капсуле сустава. Мельчайшие частицы металлов обнаруживаются не только в периартикулярных мышцах, бедренной кости, костном цементе, но и во внутренних органах. Исследования в гуманитарной медицине показали, что концентрация кобальта и хрома в легких, почках, печени и селезенке человека с эндопротезом тазобедренного сустава была в 50 раз выше нормы (10; 11).
Механические и физические свойства комохрома отечественного и импортного производства, представленные в таблице № 3, обусловлены химическим составом сплавов (табл. 4) и технологией производства. Повышение предела текучести и относительного удлинения при разрыве в комохроме импортного производства обусловлено высоким процентным содержанием никеля (Ni). Низкое содержание углерода в швейцарском комохроме должно было сказаться на пределе прочности имплантата и уменьшении его износостойкости. Компенсировали этот недостаток карбиды Сг и Мо, равномерно инкорпорированные в матрикс. Предел прочности швейцарского комохрома составил 1160 МПа. Комохром ГЭП «ЦИТО» с более высоким содержанием углерода показал меньшую износостойкость и предел прочности (700 МПа). Более низкие механические параметры и физические свойства отечественного комохрома обусловлены несовершенной технологией производства металла, неравномерным распределением карбидов-»гигантов», древоподобной структурой металла, наличием пустотелых пор.
ЗАКЛЮЧЕНИЕ
Лабораторные моделирующие исследования по определению коэффициента трения и линейного износа в узле трения эндопротезов тазобедренного сустава для собак достаточно четко указывают на преимущество имплантатов швейцарской фирмы MATHYS.
Трибологические свойства узла трения эндопротезов зависят от технологии производства и структуры металла, которые определяют качество шлифовки трущихся поверхностей имплантата, коэффициент трения и линейный износ.
Металлоз периартикулярных тканей, вызванный продуктами износа, гораздо выше у собак с имплантатами ГЭП «ЦИТО».
Морфологические исследования периартикулярных тканей у собак с двумя типами эндопротезов соотносятся с результатами анализа лабораторного моделирования, что дает основание предполагать о более высокой вероятности развития асептической нестабильности при имплантировании эндопротезов ГЭП «ЦИТО».
Авторы выражают благодарность за консультации при написании статьи член — корреспонденту РАН, доктору технических наук, профессору, заведующему кафедрой «Материаловедения и технологии обработки материалов» Российского государственного технологического университета им. К.Э. Циолковского (МАТИ) А. А. Ильину и ученому секретарю Российского государственного технологического университета им. К. Э. Циолковского (МАТИ), кандидату технических наук С. В. Скворцовой.
———————————
*Трибология (греч. Tribien, тереть; logos, учение) [англ. tribology]. Учение о трении и износе (в патологии суставов). В техническом понимании — это научная дисциплина, занимающаяся изучением трения и износа узлов машин и механизмов в присутствии смазочных материалов.
**Аустенит (от имени англ. металлурга У. Робертса-Остена, W. Roberts-Austen; 1843-1902), структурная составляющая железоуглеродистых сплавов — твердый раствор углерода (до 20%), а также лигирующих элементов в гамма-железе. В углеродистых сталях и чугунах устойчив выше 723° С.
***Эвтектика (гр. Eutektos — легко плавящийся), жидкая фаза (расплав), находящаяся в равновесии с двумя или более твердыми фазами. Температура кристаллизации Э. называется эвтектической точкой. Продукт кристаллизации жидкой Э. — твердая Э., высокодисперсная смесь нескольких твердых фаз того же состава, что и у жидкой Э.
Доброго здоровья,Валентин Львович!!! Скажите пожалуйста,как можно(какие исследования,анализы надо провести?)предусмотреть, предотвратить развитие металлоза до операции металлоостеосинтеза, до его появления?Что требуется от пациента? Что требуется от врача? Какие результаты исследований необходимо сделать? Если возможно ссылку на источник для прочтения.Заранее благодарен.С огромным уважением и признательностью!