Легочная вено - окклюзионная болезнь (ЛВОБ)- редкое заболевание не установленной этиологии, при котором развитие и прогрессирование ЛГ связано с поражением мелких легочных вен и венул, в том числе тромботического характера.
Ранее ЛВОБ рассматривалась как подтип первичной легочной гипертензии (ПЛГ), однако с учетом вероятных различий в патогенезе ЛВОБ и лечении ПЛГ, в 1998г. ЛВОБ была включена в категорию легочной венозной гипертензии наряду с заболеваниями левых отделов сердца, компрессией легочных вен, фиброзирующим медиастинитом. В 2003г. на 3-м Мировом симпозиуме по ЛГ в Венеции (Италия) на основании сходных патоморфологических проявлений, клинической картины и возможного развития отека легких при назначении простагландинов ЛВОБ и легочный капиллярный гемангиоматоз- доброкачественное неметастазирующее сосудистое образование, приводящее к развитию ЛГ- были объединены в один подтип клинического класса легочной артериальной гипертензии.


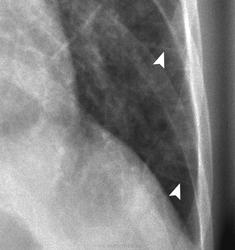
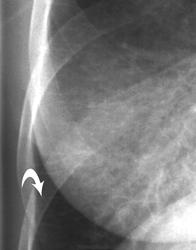
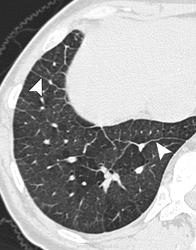

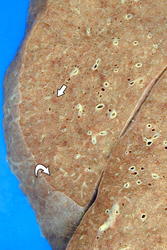
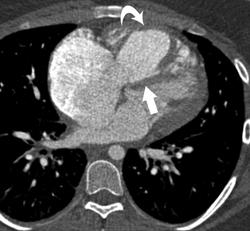
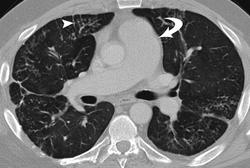
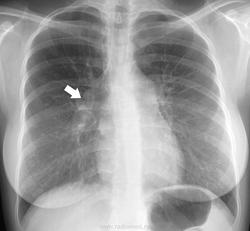
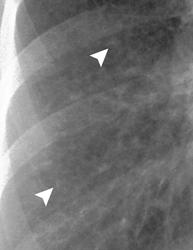
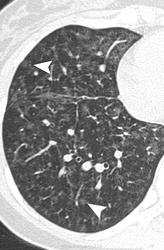
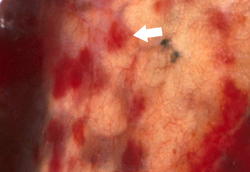


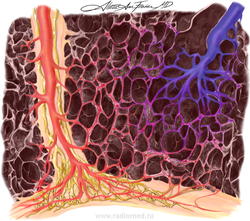
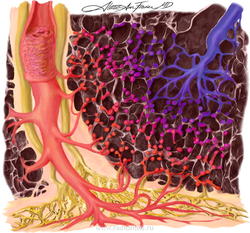
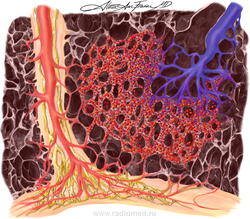
Легочный капиллярный гемангиоматоз
http://old.consilium-medicum.com/media/cardio/07_01/37.shtml